题目内容
现有如下两个反应:
A、2NaOH+H2SO4═Na2SO4+2H2O
B、CH4+2O2═CO2+2H2O
(1)根据反应的本质,两个反应都为
A
(2)如果不能,说明其理由
(3)如果能,最好应选择
A、2NaOH+H2SO4═Na2SO4+2H2O
B、CH4+2O2═CO2+2H2O
(1)根据反应的本质,两个反应都为
放热
放热
反应(放热或吸热),判断两个反应能否设计为原电池?(能或不能)A
不能
不能
B能
能
(2)如果不能,说明其理由
A的反应为非氧化还原反应,无电子转移
A的反应为非氧化还原反应,无电子转移
(3)如果能,最好应选择
NaOH
NaOH
电解质溶液(NaOH或H2SO4).则负极电极反应式:CH4-8e-+10OH-═CO32-+7H2O
CH4-8e-+10OH-═CO32-+7H2O
正极电极反应式:2O2+8e-+4H2O═8OH-
2O2+8e-+4H2O═8OH-
.分析:(1)中和反应、物质的燃烧反应是放热反应,自发的氧化还原反应能设计成原电池;
(2)自发的氧化还原反应能设计成原电池;
(3)燃料电池的放电规律:负极是燃料失电子的过程,正极是氧气得电子的过程来回答.
(2)自发的氧化还原反应能设计成原电池;
(3)燃料电池的放电规律:负极是燃料失电子的过程,正极是氧气得电子的过程来回答.
解答:解:(1)中和反应、物质的燃烧反应均是放热反应,A不是自发的氧化还原反应不能设计成原电池,B是自发的氧化还原反应能设计成原电池,故答案为:放热;不能;能;
(2)A的反应为复分解反应,属于非氧化还原反应,无电子转移,只有自发的氧化还原反应能设计成原电池,故答案为:A的反应为非氧化还原反应,无电子转移;
(3)甲烷燃料电池中,负极是甲烷燃料失电子的过程,正极是氧气得电子的过程,电极反应分别为:负极 CH4-8e-+10 OH-═CO32-+7H2O,正极 2O2+8e-+4H2O═8 OH-,为了保证放电的充分进行,可以选择碱来作电解质溶液,故答案为:NaOH;CH4-8e-+10OH-═CO32-+7H2O;2O2+8e-+4H2O═8OH-.
(2)A的反应为复分解反应,属于非氧化还原反应,无电子转移,只有自发的氧化还原反应能设计成原电池,故答案为:A的反应为非氧化还原反应,无电子转移;
(3)甲烷燃料电池中,负极是甲烷燃料失电子的过程,正极是氧气得电子的过程,电极反应分别为:负极 CH4-8e-+10 OH-═CO32-+7H2O,正极 2O2+8e-+4H2O═8 OH-,为了保证放电的充分进行,可以选择碱来作电解质溶液,故答案为:NaOH;CH4-8e-+10OH-═CO32-+7H2O;2O2+8e-+4H2O═8OH-.
点评:本题考查学生原电池的工作原理知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案
相关题目
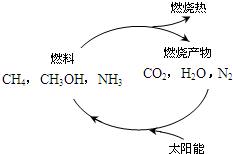 能源是当今社会发展的三大支柱之一.
能源是当今社会发展的三大支柱之一.