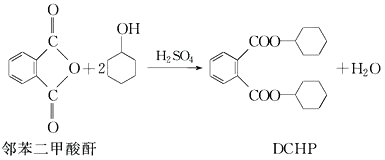
题目内容
【题目】常温下,下列各组离子在指定溶液中一定能大最共存的是( )
A.能使酚酞变红色的溶液中:Na+、Al3+、SO42-、Cl-
B.![]() 的溶液中:NH4+、Ca2+、Cl-、NO3-
的溶液中:NH4+、Ca2+、Cl-、NO3-
C.能与Al 反应放出H2的溶液中:Fe2+、K+、SO42-、NO3-
D.水电离的c(H+)=1×10-3mol/L的溶液中:K+、Na+、AlO2-、SO42-
【答案】B
【解析】A.能使酚酞变红色的溶液是碱性溶液,在碱性溶液中:OH-、Al3+会发生反应形成AlO2-和水,不能大量共存,不符合题意;
B. ![]() 的溶液是酸性溶液,在酸性溶液中,H+与NH4+、Ca2+、Cl-、NO3-不能发生任何反应,可以大量共存,符合题意;
的溶液是酸性溶液,在酸性溶液中,H+与NH4+、Ca2+、Cl-、NO3-不能发生任何反应,可以大量共存,符合题意;
C.能与Al 反应放出H2的溶液可能显酸性,也可能显碱性,在碱性溶液中:Fe2+、OH-会发生反应,不能大量共存;在酸性溶液中,H+与Fe2+、NO3-会发生氧化还原反应,不能大量共存,并且不能反应产生氢气,不符合题意;
D.水电离的c(H+)=1×10-3mol/L的溶液可能显酸性,也可能显碱性,在酸性溶液中:H+、AlO2-会反应产生Al3+ , 不能大量共存,不符合题意。
所以答案是:B

 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案【题目】已知数据:
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 |
乙醇 | -117.3 | 78.5 | 0.789 |
乙酸 | 16.6 | 117.9 | 1.05 |
乙酸乙酯 | -83.6 | 77.5 | 0.90 |
浓硫酸(98%) | — | 338.0 | 1.84 |
实验室制取乙酸乙酯的主要步骤如下:①在30 mL的大试管A中按体积比1∶4∶4的比例配制浓硫酸、乙醇和乙酸的混合溶液;②按图1连接好装置(装置气密性良好),用小火均匀地加热装有混合液的大试管3~5 min;③待试管B收集到一定量产物后停止加热,撤去试管B并用力振荡,然后静置分层;

图1
④分离出乙酸乙酯层、洗涤和干燥。
请根据题目要求回答下列问题:
(1)写出制取乙酸乙酯的化学方程式:________________________________________________________________________。
(2)上述实验中饱和碳酸钠溶液的作用是______(填字母代号)。
A.反应掉乙酸和乙醇
B.反应掉乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)步骤②中需要用小火均匀加热,其主要原因是________________________________________________________________________。
(4)某化学课外小组设计了图2所示的制取乙酸乙酯的装置(铁架台、铁夹、加热装置均已略去),
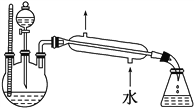
图2
与图1所示装置相比,此装置的主要优点有________________________________________________________________。