题目内容
硅是元素周期表中第14号元素,能正确表示硅的原子结构示意图的是( )
A、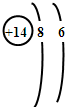 |
B、 |
C、 |
D、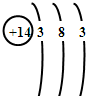 |
考点:原子结构示意图
专题:化学用语专题
分析:由硅的原子序数=核电荷数=质子数=原子核外电子数=14,依据核外电子排布规则,第一层2个电子、第二层8个电子、第三层4个电子.
解答:
解:硅是元素周期表中第14号元素,原子核内有14个质子,原子核外电子数为14,依据核外电子排布规则,第一层2个电子、第二层8个电子、第三层4个电子,
故选C.
故选C.
点评:本题考查原子结构示意图的书写,掌握原子结构和核外电子排布规则是正确书写原子结构示意图的关键.

练习册系列答案
相关题目
几种短周期元素的原子半径及主要化合价如下表,相关说法正确的是( )
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、离子半径大小:r(M3+)>r(T2-) |
| B、其中R的金属性最强 |
| C、煤和石油中存在X元素 |
| D、L、X形成的简单离子核外电子数相等 |
下列离子在pH=2的溶液中能大量共存的是( )
| A、Na+、Ba2+、SO42- |
| B、K+、Cl-、CO32- |
| C、Al3+、NO3-、SO42- |
| D、Fe3+、OH-、NO3- |
在一定条件下,将0.1L CO、0.2L CO2、0.1L NO、0.2L NO2和0.2L NH3混合,然后通过分别盛有足量蒸馏水、饱和碳酸氢钠溶液和氢氧化钠溶液的三个洗气瓶(洗气瓶排列顺序不确定).假设气体通过每个洗气瓶都能充分反映,则尾气(已干燥)( )
| A、不可能是单一气体 |
| B、不可能含有一氧化碳 |
| C、可能存在原气体中的两种气体 |
| D、成分与洗气瓶的排列顺序无关 |
金属的冶炼常涉及氧化还原反应.由下列物质冶炼相应金属时采用电解法的是( )
| A、Al2O3 |
| B、HgO |
| C、Cu2S |
| D、Fe2O3 |
下列与有机物结构、性质相关的叙述错误的是( )
A、乙醛和丙烯醛(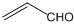 )不是同系物,但它们与H2充分反应后的产物是同系物 )不是同系物,但它们与H2充分反应后的产物是同系物 |
B、一分子β-月桂烯(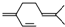 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |
C、用甘氨酸(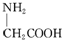 )和丙氨酸( )和丙氨酸(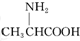 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
D、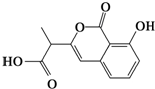 和 和 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 |
矿石中金的含量很低,金的性质又相当稳定,只能用湿法冶金--氰化法提炼,即采用稀的NaCN溶液处理已粉碎的矿石,把少量的金浸入溶液中,然后用金属锌作还原剂将金从溶液中置换析出.其反应原理为
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn═2Au+Na2[Zn(CN)4].
以下有关氰化法提炼金的说法中正确的是( )
①4Au+8NaCN+O2+2H2O═4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn═2Au+Na2[Zn(CN)4].
以下有关氰化法提炼金的说法中正确的是( )
| A、Na[Au(CN)2]不溶于水 |
| B、化合物Na[Au(CN)2]中金元素的化合价为+1 |
| C、金元素在地壳中能以化合态的形式存在 |
| D、在提炼过程中含金元素的物质始终作氧化剂 |
