题目内容
5.现有金属单质A、B和气体甲、乙、丙及物质C、D它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:ANa、丙HCl
(2)画出丙溶液中阴离子的结构示意图

(3)写出下列反应化学方程式,如果是氧化还原反应的请用双线桥标出电子转移的方向和数目.
反应①

反应⑤FeCl3+3NaOH═Fe(OH)3↓+3NaCl.
分析 金属单质A的焰色反应为黄色,应为Na,与水反应生成的气体甲为H2,C为NaOH,黄绿色气体乙为Cl2,则丙为HCl,丙溶液为盐酸,红褐色沉淀H为Fe(OH)3,则B为Fe,D为FeCl3,结合物质的性质解答该题.
解答 解:金属单质A的焰色反应为黄色,应为Na,与水反应生成的气体甲为H2,C为NaOH,黄绿色气体乙为Cl2,则丙为HCl,丙溶液为盐酸,红褐色沉淀H为Fe(OH)3,则B为Fe,D为FeCl3,
(1)根据上面的分析可知,A 为Na、丙为HCl,
故答案为:Na;HCl;
(2)丙溶液中阴离子为氯离子,其结构示意图为 ,
,
故答案为: ;
;
(3)反应①为钠与水反应生成氢氧化钠和氢气,用双线桥标出电子转移的方向和数目,反应的方程式为 ,
,
反应⑤为氢氧化钠与氯化铁反应生成氢氧化铁,反应的方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl,
故答案为: ;FeCl3+3NaOH═Fe(OH)3↓+3NaCl.
;FeCl3+3NaOH═Fe(OH)3↓+3NaCl.
点评 本题考查无机物的推断,题目难度中等,解答本题的关键是能根据物质的特性如颜色为突破口进行推断,答题时注意体会.

练习册系列答案
相关题目
16.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 常温常压下,11.2LNH3所含的原子数为2NA | |
| B. | 常温常压下,80gSO3含有的氧原子数为3NA | |
| C. | 标准状况下,22.4LH2中所含原子数为NA | |
| D. | 2 L0.3 mol•L-1 Na2SO4溶液中含0.6NA个Na+ |
20.下列贮存化学试剂的方法正确的是( )
| A. | 新制的氯水保存在棕色广口瓶中,并放在阴凉处 | |
| B. | 用做感光片的溴化银贮存在无色试剂瓶中 | |
| C. | 烧碱溶液放在带磨口玻璃塞的试剂瓶中 | |
| D. | 1mol/L NaCl溶液不能长期保存在容量瓶中 |
10.下列说法正确的是( )
| A. | ${\;}_{8}^{16}$O、${\;}_{8}^{18}$O为不同的核素,有不同的化学性质 | |
| B. | H2、SO2、NH3三种气体都可用浓硫酸干燥 | |
| C. | 分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 | |
| D. | 陶瓷、玻璃、水泥、大理石的主要成分都是硅酸盐 |
14.用53g Na2CO3固体配成2L溶液,则Na2CO3的物质的量浓度为( )
| A. | 0.25mol•L-1 | B. | 0.50mol•L-1 | C. | 0.75mol•L-1 | D. | 1.25mol•L-1 |
15.镍镉电池是一种可充电电池,该电池放电时的总反应为:Cd+2NiOOH+2H2O=Cd(OH)2+2Ni(OH)2 下列说法错误的是( )
| A. | 该电池的电解液可以选用KOH溶液,负极是Cd,正极是NiOOH | |
| B. | 该电池放电时,负极反应为:Cd-2e-+2OH-=Cd(OH)2 | |
| C. | 该电池充电过程中,阴极附近的溶液PH降低 | |
| D. | 该电池充电时,阳极反应为:2Ni(OH)2-2e-+2OH-=2NiOOH+2H2O |
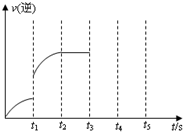 一定温度下在体积为5L的密闭容器中发生可逆反应.
一定温度下在体积为5L的密闭容器中发生可逆反应. 氢能被视作连接化石能源和可再生能源的重要桥梁.
氢能被视作连接化石能源和可再生能源的重要桥梁. ;与氨硼烷互为等电子体的有机化合物是CH3CH3(写结构简式).
;与氨硼烷互为等电子体的有机化合物是CH3CH3(写结构简式). .
. ;镁条在气体B中燃烧生成的物质是Mg3N2(填化学式);
;镁条在气体B中燃烧生成的物质是Mg3N2(填化学式);