题目内容
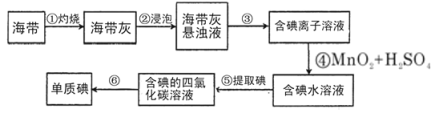
【题目】海带含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
请填写下列空白:
(1)步骤③的实验操作名称是________,该操作用到的玻璃仪器有烧杯,_________,________。
(2)步骤⑤用到的玻璃仪器除烧杯外还有____________,能否用乙醇来代替CCl4________(填“能”或“否”)。
(3)步骤⑥的实验操作名称是________。
(4)步骤③得到的滤液中c(I-)=0.04mol/L,欲使用c(I-)=0.01mol/L的溶液480mL,需取用该滤液________mL。下列操作会使配制的溶液的物质的量浓度偏小的是_________。
A.稀释溶液时有液体溅出 B.容量瓶中有少量蒸馏水残留
C.取滤液时仰视刻度线 D.向容量瓶中加水定容时仰视刻度线
【答案】过滤 漏斗 玻璃棒 分液漏斗 否 蒸馏 125 AD
【解析】
(1)不溶于水的物质需要过滤分离,根据过滤操作来分析用到的实验仪器;
(2)步骤⑤为从碘水中萃取碘单质,需要萃取分液,用到分液漏斗;根据萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多分析;
(3)步骤⑥的目的是从含碘的四氯化碳溶液中分离出单质碘和回收四氯化碳,利用沸点的差异用蒸馏的方法;
(4)配制480mL溶液需要500mL容量瓶,结合c=n/V和实验操作分析可能产生的误差。
(1)步骤③是从海带灰的悬浊液中得到含碘离子的溶液,其实验操作名称是过滤,该操作用到的玻璃仪器有烧杯、漏斗、玻璃棒;
(2)步骤⑤为从碘水中萃取碘单质,需要萃取分液,用到的玻璃仪器除烧杯外还有用到分液漏斗。由于乙醇和水互溶,所以不能用乙醇来代替CCl4;
(3)步骤⑥的目的是从含碘的四氯化碳溶液中分离出单质碘和回收四氯化碳,是利用互溶的两种液体的沸点不同来分离,则实验操作为蒸馏;
(4)步骤③得到的滤液中c(I-)=0.04mol/L,欲使用c(I-)=0.01mol/L的溶液480mL,由于需要使用500mL容量瓶,因此需取用该滤液的体积为![]() =125mL。
=125mL。
A.稀释溶液时有液体溅出,溶质的物质的量减少,浓度偏小;
B.容量瓶中有少量蒸馏水残留不影响溶质的物质的量和溶液体积,浓度不变;
C.取滤液时仰视刻度线导致实际量取的体积增加,所以浓度偏大;
D.向容量瓶中加水定容时仰视刻度线,溶液体积增加,浓度偏小。
答案选AD。

 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案【题目】下表是三种难溶金属硫化物的溶度积常数(25 ℃):下列有关说法中正确的是
化学式 | FeS | CuS | MnS |
溶度积 | 6.3×10-18 | 1.3×10-36 | 2.5×10-13 |
A. 25 ℃时,将CuS固体用含Mn2+的饱和溶液浸泡可溶解CuS固体
B. 25 ℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-36 mol·L-1
C. 除去某溶液中的Cu2+,可以选用FeS作沉淀剂
D. 因为H2SO4是强酸,所以反应CuSO4+H2S===CuS↓+H2SO4不能发生