题目内容
【题目】某同学用以下装置制备并检验Cl2的性质。下列说法正确的是( )
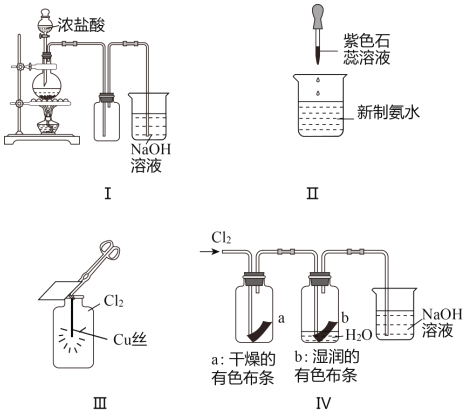
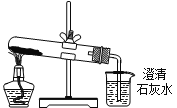
A. 图Ⅰ:若MnO2过量,则浓盐酸可全部消耗完 B. 图Ⅱ:证明新制氯水具有酸性
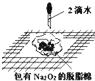
C. 图Ⅲ:产生了棕黄色的雾 D. 图Ⅳ:湿润的有色布条褪色
【答案】D
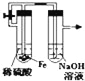
【解析】分析:A.根据稀盐酸与二氧化锰不反应分析;
B.依据氯水中含有氢离子、次氯酸分子,具有酸性和漂白性解答;
C.化学中的烟为固体小颗粒,雾为小液滴;
D.氯气不具有漂白性,次氯酸具有漂白性.
详解:A.二氧化锰与浓盐酸反应,随着反应的进行,浓盐酸变稀,二氧化锰不与稀盐酸反应,即使二氧化锰过量,盐酸也不能全部消耗完,A错误;
B.图Ⅱ中溶液先变红后褪色,不仅能证明新制氯水具有酸性,还可以证明新制氯水具有漂白性,B错误;
C.铜丝在氯气中燃烧,生成棕黄色的烟,不是雾,C错误;
D.氯气没有漂白性,图Ⅳ中氯气遇到湿润有色布条与水反应生成HClO,HClO具有漂白性,可使有色布条褪色,D正确;答案选D。

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目