题目内容
【题目】在N2F2分子中,所有原子均符合8电子稳定结构,则该分子中的共价键类型是
A. 仅有σ键 B. 三个σ键,两个π键
C. 两个σ键,两个π键 D. 三个σ键,一个π键
【答案】D
【解析】
由题所给条件,在N2F2分子中,所有原子均符合8电子稳定结构可知,其结构式应为:F-N=N-F,两个氮之间是氮氮双键,一个为σ键一个为π键,氮氟之间是单键,为σ键,所以该分子中的共价键类型是三个σ键,一个π键。故D正确。
综上所述,本题应选D。

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
【题目】将下列有关内容依次填入下图各框中,其中包含关系正确的选项是( )
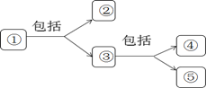
| ① | ② | ③ | ④ | ⑤ |
A | 生物大分子 | 蛋白质 | 核酸 | 脱氧核糖核苷酸 | 核糖核苷酸 |
B | 脂质 | 脂肪 | 胆固醇 | 性激素 | 维生素D |
C | 单糖 | 五碳糖 | 六碳糖 | 葡萄糖 | 乳糖 |
D | 无机物 | 无机盐 | 水 | 自由水 | 结合水 |
A. A B. B C. C D. D