题目内容
1.下列说法正确的是( )①Al和Fe可用于做建筑材料,也可用于制作饮料罐;
②Al和Fe表面在空气中都可自然生成一层致密的氧化膜,保护内层金属不被腐蚀;
③Al2O3和Fe2O3都为碱性氧化物,所以都能溶于硫酸;
④Al(OH)3与Fe(OH)3加热都会分解,生成对应的氧化物.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
分析 ①Al、Fe具有良好的延展性,可用于制作饮料罐,Al被氧化生成的氧化铝熔点高,可作耐火材料,铁冶炼得到钢筋用于建筑材料;
②铁和氧气生成的是铁锈,不是致密的氧化膜,Al表面在空气中都可自然生成一层致密的氧化膜;
③氧化铝是两性氧化物,氧化铁为碱性氧化物;
④氢氧化铝分解生成氧化铝和水,氧化铁分解生成氧化铁和水;
解答 解:①Al、Fe具有良好的延展性,可用于制作饮料罐,Al被氧化生成的氧化铝熔点高,可作耐火材料,铁冶炼得到钢筋用于建筑材料,Al和Fe可用于做建筑材料,也可用于制作饮料罐,故①正确;
②表面在空气中铁和氧气生成的是铁锈,不是致密的氧化膜,Al表面在空气中都可自然生成一层致密的氧化膜,故②错误;
③氧化铝是两性氧化物,氧化铁为碱性氧化物,都能溶于硫酸,故③错误;
④氢氧化铝分解生成氧化铝和水,氧化铁分解生成氧化铁和水,Al(OH)3与Fe(OH)3加热都会分解,生成对应的氧化物,故④正确;
故选C.
点评 本题考查Al的性质,为高频考点,综合考查元素化合物知识,把握物质的性质及发生的反应为解答的关键,注意性质与用途的关系,题目难度不大.

练习册系列答案
相关题目
11.用下列实验装置或操作进行的实验能达到实验目的是( )
| A. | 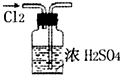 干燥Cl2 干燥Cl2 | B. | 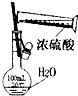 配制100ml 0.1mol•L-1硫酸溶液 | ||
| C. | 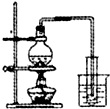 制取少量蒸馏水 | D. |  检验钾元素的存在 |
12.要从硝酸钾和食盐(少量)的混合物中,分离出较纯净的硝酸钾,应把它们( )
| A. | 溶解、过滤 | |
| B. | 制成热的硝酸钾饱和溶液,降温后再过滤 | |
| C. | 制成溶液后直接蒸干 | |
| D. | 先溶解、再蒸发结晶,趁热过滤 |
9.在80℃时,水的离子积为1.6×10-13,若该温度下某溶液中的c(H+)为1×10-7mol/L,则该溶液( )
| A. | 呈碱性 | B. | 呈酸性 | C. | 呈中性 | D. | c(OH-)=10c(H+) |
4.在容积固定为2L的密闭容器中,充入0.180molHI,480℃时反应:2HI(g)?H2(g)+I2(g),体系中n(HI)随时间变化情况如下表:
反应进行至10min后将反应混合物的温度降低,发现气体的颜色变浅.
(1)0~2min内H2的平均反应速度为0.002mol/(L•min).达平衡时,HI的转化率是22.2%.
(2)当上述反应达平衡时,降低温度,原化学平衡向逆向移动(填“正向”,“逆向”或“不”),上述正向反应是:吸热反应(选填:放热、吸热),逆反应速率减小(填“增大”、“减小”或“不变”).
(3)480℃时,反应H2(g)+I2(g)?2HI(g)的平衡常数K的值为49.
(4)要增大反应2HI(g)?H2(g)+I2(g)的平衡常数,可采取的措施是D(选填字母).
A.增大HI起始浓度 B.向混合气体中通入I2 C.使用高效催化剂 D.升高温度.
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(HI)/mol | 0.180 | 0.164 | 0.152 | 0.144 | 0.140 | 0.140 |
(1)0~2min内H2的平均反应速度为0.002mol/(L•min).达平衡时,HI的转化率是22.2%.
(2)当上述反应达平衡时,降低温度,原化学平衡向逆向移动(填“正向”,“逆向”或“不”),上述正向反应是:吸热反应(选填:放热、吸热),逆反应速率减小(填“增大”、“减小”或“不变”).
(3)480℃时,反应H2(g)+I2(g)?2HI(g)的平衡常数K的值为49.
(4)要增大反应2HI(g)?H2(g)+I2(g)的平衡常数,可采取的措施是D(选填字母).
A.增大HI起始浓度 B.向混合气体中通入I2 C.使用高效催化剂 D.升高温度.
8.卤素单质及化合物在许多性质上都存在着递变规律.下列有关说法不正确的是( )
| A. | 卤素单质的沸点按F2、Cl2、Br2、I2的顺序依次增大 | |
| B. | 卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由易变难 | |
| C. | 卤化氢的热稳定性和还原性按HF、HCl、HBr、HI的顺序依次减弱 | |
| D. | 卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深 |
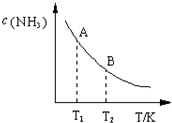 氨在国民经济中占有重要地位.请回答有关氨的下列问题:
氨在国民经济中占有重要地位.请回答有关氨的下列问题: