题目内容
将两个铂电极插人KOH溶液中,向两极分别通人CH4和O2,构成甲烷燃料电池。已知。通人CH4的一极,其电极反应式是:CH4 + 10OH- - 8e-=CO32-+7 H2O;通入O2的另一极,其电极反应式是:2O2 + 4H2O +8e- = 8OH-。下列叙述不正确的是( )。
| A.通人CH4的电极为负极 |
| B.正极发生氧化反应 |
| C.燃料电池工作时,溶液中的OH-向负极移动 |
| D.该电池使用一段时间后应补充KOH |
B
试题分析:原电池中负极失去电子,发生氧化反应。正极得到电子,发生还原反应,所以甲烷在负极通入,氧气在正极通入,因此A正确,B不正确;根据电极反应式可知,选项C和D都是正确的,答案选B。
点评:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应,据此可以进行有关的判断和计算。

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
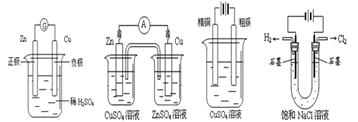
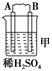

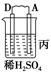
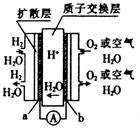
 NiOOH+MH,下列叙述正确的是
NiOOH+MH,下列叙述正确的是