题目内容
8.取少量MgO、Al2O3、SiO2、Fe2O3的混合粉末,加入过量盐酸,充分反应后过滤,得到沉淀X和滤液Y.下列叙述正确的是( )| A. | 上述四种氧化物中,只有SiO2是酸性氧化物,它不溶于任何酸 | |
| B. | 向沉淀X中逐滴加入硝酸,沉淀慢慢溶解 | |
| C. | 溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+ | |
| D. | 溶液Y中加入过量氨水,所得沉淀为Fe(OH)3和Mg(OH)2 |
分析 A、二氧化硅可溶于氢氟酸;
B、沉淀X为SiO2,不溶于硝酸;
C、溶液Y为氯化镁、氯化铝、氯化铁、盐酸溶液;
D、氢氧化铝是两性氢氧化物,不溶于弱酸弱碱.
解答 解:A、上述四种氧化物中,只有SiO2是酸性氧化物,二氧化硅可溶于氢氟酸,故A错误;
B、MgO、Al2O3、SiO2、Fe2O3的混合粉末,加入过量盐酸,氧化镁、氧化铝、氧化铁溶解,二氧化硅不溶,沉淀X为SiO2,不溶于硝酸,故B错误;
C、溶液Y为氯化镁、氯化铝、氯化铁、盐酸溶液,溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+,故C正确;
D、氢氧化铝是两性氢氧化物,不溶于弱酸弱碱,溶液Y中加入过量氨水,所得沉淀为Fe(OH)3、Al(OH)3和Mg(OH)2,故D错误;
故选C.
点评 本题考查了物质性质的制备,除杂方法,物质性质的理解应用,主要是两性物质性质的判断,掌握基础是解题关键,题目难度中等.

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
18.有下列几种反应类型:①消去②取代③水解④加成⑤氧化,用丙醇制取1,2-丙二醇,按正确的合成路线依次发生的反应所属类型应是( )
| A. | ①④③ | B. | ⑤④③ | C. | ②①③ | D. | ②①④ |
19.下列叙述正确的是( )
| A. | 粗铜提纯时以硫酸铜溶液作电解液,精铜作阳极 | |
| B. | 铁钉镀铜时铁钉做阴极,发生氧化反应 | |
| C. | 用惰性电极电解CuSO4溶液一段时间后再加入纯净的CuO,可以使溶液恢复到原来的成分和浓度 | |
| D. | 粗铜提纯时电解后Fe、Zn、Ag等杂质会沉积在电解槽底部形成阳极泥 |
16.以下离子方程式书写正确的是( )
| A. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| B. | 稀NH4Cl溶液和稀NaOH溶液作用:NH4++OH-═NH3↑+H2O | |
| C. | 氨气通入醋酸溶液中:CH3COOH+NH3═CH3COONH4 | |
| D. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- |
3.从有机化合物的分类来看,下列反应中的X属于( )
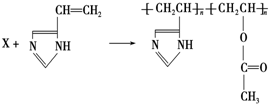

| A. | 醇 | B. | 烷烃 | C. | 烯烃 | D. | 酯 |
17.用惰性电极电解Fe2(SO4)3和CuSO4的混合溶液,下列说法正确的是( )
| A. | 阴极反应式为:Cu2++2e-═Cu,当有Cu2+存在时,Fe3+不放电 | |
| B. | 阴极上首先析出铁,然后析出铜 | |
| C. | 阴极先是Fe3+放电,后Cu2+放电 | |
| D. | 阴极上不可能析出铜 |
18.下列叙述中错误的是( )
| A. | 原子半径 Na>Si>Cl | B. | 金属性 Na>Mg>Al | ||
| C. | 稳定性 SiH4<HCl<H2S | D. | 酸性 H3PO4<H2SO4<HClO4 |
 HClO+OH-
HClO+OH-