题目内容
【题目】已知下列两个气态物质之间的反应:C2H2(g)+H2(g)![]() C2H4(g) ①
C2H4(g) ①
2CH4(g)![]() C2H4(g)+2H2(g) ②
C2H4(g)+2H2(g) ②
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:(Q1、Q2、Q3均为正值)
C(s)+2H2(g)=CH4(g) ΔH=-Q1 I
2C(s)+H2(g)=C2H2(g) ΔH=-Q2 II
2C(s)+2H2(g)=C2H4(g) ΔH=-Q3 III
Q值大小比较正确的是
A.Q1>Q3>Q2 B.Q1>Q2>Q3 C.Q2>Q1>Q3 D.Q3>Q1>Q2
【答案】A
【解析】
试题分析:当温度降低时,反应①的平衡向正反应方向移动,说明该反应正向为放热反应,△H<0,反应②的平衡向逆反应方向移动,说明该反应正向为吸热反应,△H>0,
已知下列两个气态物质之间的反应:C2H2(g)+H2(g)C2H4(g)…①,
2CH4(g)C2H4(g)+2H2(g)…②,
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
(1)C(s)+2H2(g)CH4(g),△H=-Q1…Ⅰ
(2)C(s)+1/2H2(g)1/2C2H2(g),△H=-Q2…Ⅱ
(3)C(s)+H2(g)1/2C2H4(g),△H=-Q3…Ⅲ,
利用盖斯定律,2×[(3)-(2)],得到C2H2(g)+H2(g)C2H4(g),△H=2(Q2-Q3),
与题干中的①中的方程式一样,而①中的反应为放热反应,则Q2-Q3<0,所以Q2<Q3;
同理:2×[(3)-(1)],得到2CH4(g)C2H4(g)+2H2(g),△H=2(Q1-Q3),与题干中的②中的方程式一样,而②中的反应为吸热反应,则2(Q1-Q3)>0,所以Q1>Q3;
综上所述Q1>Q3>Q2.故选A。

【题目】下列有关反应热的叙述中正确的是
①已知2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1,则氢气的燃烧热为△H=-241.8kJ·mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)![]() Z(g)+W(s) △H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
Z(g)+W(s) △H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
④已知:
共价键 | C—C | C=C | C—H | H—H |
键能/(kJ·mol-1) | 348 | 610 | 413 | 436 |
上表数据可以计算出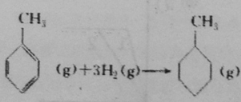 的焓变
的焓变
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量相等
⑥25℃,101kPa,1mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热
A.①②③④ B.③④⑤ C.④⑤ D.⑥