��Ŀ����
����Ŀ����ͼ1��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص������Լ���ǩ�ϵIJ������ݣ� 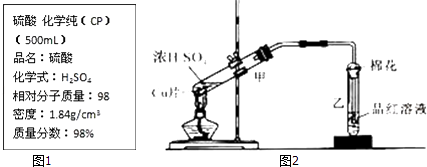
��1�����������A��D��ʾ�����ʣ����¹�����Ҫ������Ũ�������Щ���ʣ��뽫ѡ����ĸ�������и�С��������ڣ�
A���� B ��ˮ�� C ��ˮ�� D ǿ������
��Ũ������Ը�������
��Ũ����ʹľ�����
���ȵ�Ũ������ͭƬ��Ӧ
��Ũ����ʹ������Ϊ��ɫ
��2�������ø�Ũ��������100mL 1mol/L��ϡ���ᣮ�ɹ�ѡ�õ������У�
�ٽ�ͷ�ιܣ�����ƿ�����ձ�����ҩ�ף�����Ͳ����������ƽ��
��ش��������⣺
��i������ϡ����ʱ�����������в���Ҫʹ�õ�����ѡ����ţ�����ȱ�ٵIJ�����������д�������ƣ���
��ii�������㣬����100mL1mol/L��ϡ������Ҫ����Ͳ��ȡ����Ũ��������ΪmL������һλС������
��3������ͼ2ΪŨ������ͭƬ��Ӧ��װ�ã���ش�
��Ũ������ͭƬ��Ӧ�Ļ�ѧ����ʽΪ ��
�ڷ�Ӧһ��ʱ����Թ�����Ʒ����Һ�������� ��
���𰸡�
��1��B��C��AD��B
��2���ڢܢޣ�100m����ƿ����������5.4
��3��Cu+2H2SO4��Ũ�� ![]() ?CuSO4+SO2��+2H2O��Ʒ����Һ��ɫ
?CuSO4+SO2��+2H2O��Ʒ����Һ��ɫ
���������⣺��1.����Ũ������Ը�������������ΪŨ���������ˮ�ԣ���ѡ��B����Ũ����ʹľ����ڣ�����Ũ�������ˮ�ԣ���ѡ��C�����ȵ�Ũ������ͭƬ��Ӧ��������ͭ�����������ˮ�����Ჿ�ֱ���ǿ�����ԣ����ֱ������ԣ���ѡ��AD����Ũ�������յ����еĽᾧˮʹ������Ϊ��ɫ����Ũ�������ˮ�ԣ���ѡ��B��
��2.����i����100mL 1mol/L��ϡ��������Ʋ����У����㡢��ȡ��ϡ�͡���ȴ����Һ��ϴ����Һ�����ݡ�ҡ�ȵȲ�����һ������Ͳ��ȡ���õ���ͷ�ιܣ������ձ���ϡ�ͣ����ò��������裬��ȴ��ת�Ƶ�100mL����ƿ�У����ò���������������ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμӣ��μ�����Һ������̶���ˮƽ���У��Ǻ�ƿ����ҡ�ȣ���Ҫʹ�õ�����Ϊ����Ͳ���ձ�����������100mL����ƿ����ͷ�ιܣ����Բ���Ҫ������Ϊ���ڢܢޣ���ȱ�ٵ�����Ϊ����������100mL����ƿ�����Դ��ǣ��ڢܢޣ���������100mL����ƿ����ii��ͼʾ��Ũ��������ʵ���Ũ��Ϊ��c= ![]() mol/L=18.4mol/L������100mL1mol/L��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ��
mol/L=18.4mol/L������100mL1mol/L��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ�� ![]() ��0.0054L=5.4mL�����Դ��ǣ�5.4��
��0.0054L=5.4mL�����Դ��ǣ�5.4��
��3.����ͭ��Ũ�����ڼ��������·�Ӧ��������ͭ�����������ˮ������ʽ��Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O�����Դ��ǣ�Cu+2H2SO4��Ũ��
CuSO4+SO2��+2H2O�����Դ��ǣ�Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O���ڶ����������Ư���ԣ��ܹ�ʹƷ����Һ��ɫ�����Դ��ǣ�Ʒ����Һ��ɫ��
CuSO4+SO2��+2H2O���ڶ����������Ư���ԣ��ܹ�ʹƷ����Һ��ɫ�����Դ��ǣ�Ʒ����Һ��ɫ��

 ��ʱѵ���������������ϵ�д�
��ʱѵ���������������ϵ�д�
