题目内容
【题目】CH4 是一种清洁、高效、具有优良的环保性能的燃料,其燃烧热为890.3kJ·mol-1。它可以作为燃料电池的燃料。
(1)写出甲烷燃烧的热化学方程式:____________________________________________;
(2)以甲烷、空气、氢氧化钾溶液为原料,惰性电极为电极可以构成燃料电池。该电池的负极反应式为____
(3)用(2)中的燃料电池为电源,以石墨为电极电解500mL滴有酚酞的NaCl溶液,装置如图所示:
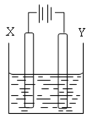
①请写出电解过程中阴极附近观察到的现象:____________________。
②当燃料电池消耗2.8L O2(标准状况下)时,计算此时NaCl溶液的pH=__________ (假设溶液的体积不变,气体全部从溶液中逸出)。在Y极通过的电子的物质的量为:_______________________。
③电解之后,要使溶液恢复原状,应该向溶液中加入物质 _________(填名称)。溶液中Cl―流向 ____________极(填“X”或“Y”)。
【答案】CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ·mol-1 CH4-8e-+10OH-=CO32-+7H2O 阴极附近变红 14 0.5mol 盐酸 阳
【解析】
(1)依据热化学方程式的书写方法,结合燃烧热的概念是1mol可燃物完全燃烧生成稳定氧化物时放出的热量写出,注意标注物质的聚集状态和燃烧热;
(2)先判断氧化剂、还原剂,然后根据原电池原理判断正负极上反应的物质,结合电解质溶液写出电极反应式;
(3)依据电源判断X为电解池的阳极,Y为电解池的阴极;
①阴极是溶液中的氢离子得到电子生成氢气,溶液中水的电离被破坏,生成了氢氧根离子显碱性,遇酚酞变红;
②根据甲烷燃料电池的电极反应和电解氯化钠的电极反应,依据电子守恒计算得到;电极上的电子转移守恒;
③依据电解氯化钠溶液生成了氢气、氯气和氢氧化钠,恢复原溶液浓度需要加入氢气和氯气组成的含氯化氢的盐酸溶液;电解过程中阴离子移向阳极。
(1)CH4 是一种清洁、高效、具有优良的环保性能的燃料,其燃烧热为890.3kJ·mol-1,热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ·mol-1,故答案为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ·mol-1;
(2)负极上的电极反应式等于电池的总反应式-正极发生的电极方程式;以甲烷、空气、氢氧化钾溶液为原料,惰性电极可构成燃料电池,正极反应为:3O2+12H2O+12e-=12OH-,总反应式为:CH4+2O2+2OH-=CO32-+3H2O,两式相减,负极反应为:CH4-8e-+10OH-=CO32-+7H2O,故答案为:CH4-8e-+10OH-=CO32-+7H2O;
(3)燃料电池为电源,以石墨为电极电解500mL滴有酚酞的NaCl溶液,X为电解池的阳极,Y为电解池的阴极;
①阴极是溶液中的氢离子得到电子生成氢气,溶液中水的电离被破坏,生成了氢氧根离子显碱性,遇酚酞变红;电解过程中阴极附近观察到的现象是,阴极附近变红,故答案为:阴极附近变红;
②甲烷燃料电池的正极消耗氧气,燃料电池消耗2.8L O2物质的量=2.8L÷22.4L·mol-1=0.125mol;正极反应为:3O2+12H2O+12e-=12OH-,计算得到电子转移为0.5mol;电解氯化钠溶液阴极电极反应为:2H++2e-=H2↑,根据水电离出的氢氧根离子和氢离子守恒,溶液中减少的氢离子和增加的氢氧根离子相同,计算得到生成氢氧根离子物质的量为0.5mol,c(OH-)=![]() =1mol·L-1;所以溶液pH=14;电极上的电子守恒得到在Y极通过的电子的物质的量为0.5mol,故答案为:14; 0.5mol;
=1mol·L-1;所以溶液pH=14;电极上的电子守恒得到在Y极通过的电子的物质的量为0.5mol,故答案为:14; 0.5mol;
③电解氯化钠溶液生成了氢气、氯气和氢氧化钠,恢复原溶液浓度需要加入氢气和氯气组成的含氯化氢的盐酸溶液;电解过程中阴离子移向阳极,故答案为:盐酸;阳。

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案【题目】乙烯的产量是衡量一个国家石油化工水平的重要标志。工业上常用丁烷裂解制备乙烯。
主反应:C4H10(g,正丁烷)![]() C2H4(g)+C2H6(g) ΔH1
C2H4(g)+C2H6(g) ΔH1
副反应:C4H10(g,正丁烷)![]() CH4(g)+C3H6(g) ΔH2
CH4(g)+C3H6(g) ΔH2
回答下列问题:
(1)化学上,将稳定单质的能量定为0,由元素的单质化合成单一化合物时的反应热叫该化合物的生成热,生成热可表示该物质相对能量。下表为25℃、101kPa下儿种有机物的生成热:
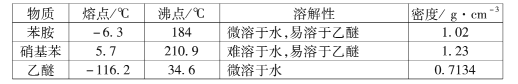
物质 | 甲烷 | 乙烷 | 乙烯 | 丙烯 | 正丁烷 | 异丁烷 |
生成热/kJ·mol-1 | -75 | -85 | 52 | 20 | -125 | -132 |
①上述反应中,ΔH1=___kJ·mol-1。
②若忽略副反应,相同条件下采用异丁烷裂解制取一定量的乙烯,其能耗比采用正丁烷__(填“高”或“低”)。
(2)一定温度下,在恒压密闭容器中投入一定量正丁烷发生反应生成乙烯。
①下列情况表明该反应达到平衡状态的是___(填代号)。
a.气体密度保持不变
b.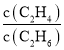 保持不变
保持不变
c.ΔH不变
d.正丁烷分解速率和乙烷消耗速率相等
②为了同时提高反应速率和转化率,可采用的措施是__。
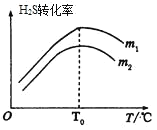
(3)向密闭容器中充入丁烷,在一定条件(浓度、催化剂及压强等)下发生反应,测得乙烯产率与温度关系如图所示。
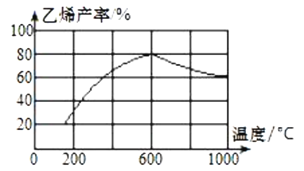
温度高于600℃时,随着温度升高,乙烯产率降低,可能的原因是__。
(4)在一定温度下向1L恒容密闭容器中充入2mol正丁烷,容器内压强为P0,反应生成乙烯和乙烷,经过10min达到平衡状态,此温度下用各组分的分压表示的平衡常数K(p)=0.5P0用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),则0~10min内乙烯的生成速率v(C2H4)为__mol·L-1。