��Ŀ����
����Ŀ������ʱ�����������Ļ����Һ20 mL������������μ���0.05mol/LBa(OH)2��Һʱ�����ɵ�BaSO4��pH�ı仯��ͼ��ʾ����������Һ���ʱ����ı仯����
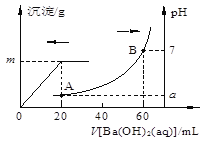
����˵����ȷ����
A.ͼ��A���Ӧ��Һ��pH��a��1
B.���ɳ������������m��2.33g
C.ԭ���Һ���������ʵ���Ũ��Ϊ0.1mol/L
D.��V[Ba(OH)2(aq)]��10mLʱ��������Ӧ�����ӷ���ʽΪ��Ba2++ SO42����BaSO4��
���𰸡�A
��������
��ͼ��֪������20mLBa��OH��2��Һʱ�����ᱵ���������ֵ����0��20mLֻ������������������Ӧ��������δ��Ӧ�����ݷ���ʽ�������ᡢ���ᱵ�����ʵ���������m=nM�������ᱵ����������ͼ��֪��pH=7ʱ������60mLBa��OH��2��Һ����H++OH-�TH2O��֪n��H+��=n��OH-�����ݴ˼���ԭ��Һ�к��е�n��H+������������ԭ��Һ��n��HCl�����ٸ���c= ![]() ����ԭ��Һ����������ʵ���Ũ�ȣ�ͼ��A������δ��Ӧ�������Ϻ������ӵ�Ũ�ȣ�����pH=-lgc��H+�����㡣
����ԭ��Һ����������ʵ���Ũ�ȣ�ͼ��A������δ��Ӧ�������Ϻ������ӵ�Ũ�ȣ�����pH=-lgc��H+�����㡣
��ͼ��֪������20mLBa��OH��2��Һʱ�����ᱵ���������ֵ��ֻ������������������Ӧ��������δ��Ӧ����ʱ�����������������ʵ���=0.02L��0.05molL-1=0.001mol����H2SO4+Ba��OH��2�TBaSO4��+H2O��n��H2SO4��=n��Ba��OH��2��=n(BaSO4)=0.001mol����ͼ��֪��pH=7ʱ������60mLBa��OH��2��Һ����ʱ�����������������ʵ���=0.06L��0.05molL-1=0.003mol����H++OH-�TH2O��֪ԭ��Һ�к��е�n��H+��=n��OH-��=0.003mol��2=0.006mol����n��HCl��=0.006mol-0.001mol��2=0.004mol��
A��A������20ml����������Һ�������ﵽ���ֵ����˵��ǡ�������ᷴӦ�������ᱵ������������������������60mLʱpH��7����˵����ʱ����ǡ�÷�Ӧ�����������������������40mL������������ʵ�����0.04L��0.05mol/L��2��0.004mol����A�������Ũ����![]() ��0.1mol/L�����ʱpH��1��A��ȷ��
��0.1mol/L�����ʱpH��1��A��ȷ��
B�����ɳ������������m��0.05mol/L��0.02L��233g/mol��0.233g��B����
C��ԭ���Һ���������ʵ���Ũ�ȣ�![]() =0.2mol/L��C����
=0.2mol/L��C����
D����V[Ba(OH)2(aq)]��10mLʱ�������������ᱵ�⣬�������������������������ˮ�����ӷ�Ӧ��D����
��ѡA��

 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д� Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д� ״Ԫ����ϵ�д�
״Ԫ����ϵ�д�