籾朕坪否
厮岑⦿HCN(aq)嚥NaOH(aq)郡哘議ΔH﹆⇩12.1 kJ,mol⇩1◉HCl(aq)嚥NaOH(aq)郡哘議ΔH﹆⇩57.3 kJ,mol⇩1⇧夸HCN壓邦卑匣嶄窮宣議ΔH吉噐 ( )。
| A⤴⇩69.4 kJ,mol⇩1 | B⤴⇩45.2 kJ,mol⇩1 |
| C⤴⇦45.2 kJ,mol⇩1 | D⤴⇦69.4 kJ,mol⇩1 |
C
盾裂

膳楼過狼双基宛
 返性返畠單膳深壌狼双基宛
返性返畠單膳深壌狼双基宛
屢購籾朕
和双企仏音嬬器欺准嬬受電朕議議頁
| A⤴旋喘湊剩嬬崙狽伴創 | B⤴喘社喘廿概旗紋巷住概 |
| C⤴旋喘咳労嬬窟窮 | D⤴喘准嬬菊旗紋易潟菊 |
和双犯晒僥圭殻塀慕亟屎鳩議頁(ΔH議蒸斤峙譲屎鳩) ( )
| A⤴C(s)⇦1/2O2(g)﹆CO(g) ΔH﹆⇩110.5kJ,mol⇩1 (伴付犯) |
| B⤴2H2O(g)﹆2H2(g)⇦O2(g) ΔH﹆⇦483.6 kJ,mol⇩1(郡哘犯) |
| C⤴C2H5OH⇦3O2﹆2CO2⇦3H2O ΔH﹆⇩1368.8 kJ,mol⇩1(郡哘犯) |
| D⤴2NaOH(aq)⇦H2SO4(aq)﹆Na2SO4 (aq)⇦2H2O(l) ΔH﹆⇩114.6 kJ,mol⇩1(嶄才犯) |
汲壓音揖彜蓑和↙耕蓑賜賑蓑⇄嚥狽賑郡哘議犯晒僥圭殻塀泌和侭幣⦿
〙H2↙g⇄ + I2↙?⇄ 2HI↙g⇄+9⤴48kJ
2HI↙g⇄+9⤴48kJ
〖H2↙g⇄ + I2↙?⇄ 2HI↙g⇄-26⤴48kJ
2HI↙g⇄-26⤴48kJ
和双登僅屎鳩議頁
| A⤴〙嶄議I2葎耕蓑⇧〖嶄議I2葎賑蓑 |
| B⤴〖議郡哘麗悳嬬楚曳〙議郡哘麗悳嬬楚詰 |
| C⤴〙議恢麗曳郡哘〖議恢麗犯糧協來厚挫 |
| D⤴1mol 耕蓑汲幅鯖扮繍簾犯17kJ |
蝶郡哘壓郡哘狛殻嶄議嬬楚延晒泌夕侭幣(夕嶄E1燕幣郡哘麗悳嬬楚,E2燕幣伏撹麗悳嬬楚)。和双嗤購偃峰屎鳩議頁( )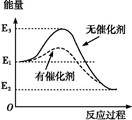
| A⤴乎郡哘葎簾犯郡哘 |
| B⤴聞喘岸晒質短嗤個延郡哘議郡哘犯 |
| C⤴郡哘犯吉噐E3-E2 |
| D⤴岸晒質峪斤屎郡哘嗤岸晒恬喘,斤剃郡哘涙岸晒恬喘 |
^詰娘将蔀 ̄頁參詰嬬債、詰麟半、詰電慧葎児粥議辛隔偬窟婢議将蔀庁塀。和双傍隈嚥^詰娘将蔀 ̄音憲栽議頁 ( )。
| A⤴寡喘儿抹爺隼賑旗紋伴嗟 |
| B⤴紗酔晒墳伴創議蝕寡嚥聞喘⇧戻互繁断議伏試邦峠 |
| C⤴旋喘壕可創崙撹高懸窟窮廾崔窟窮 |
| D⤴旋喘湊剩嬬、欠嬬吉⇧受富晒墳伴創議聞喘 |
壓匯協訳周和⇧割蛍伴付匯協楚議供莱⇧慧竃犯楚葎
Q kJ↙Q>0⇄⇧将霞協頼畠簾辺伏撹議屈剳晒娘俶勣嶧債5 mol,L-1議KOH卑匣100 mL⇧如挫伏撹屎冦⇧夸緩訳周和郡哘C4H10↙g⇄+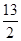 O2↙g⇄=4CO2↙g⇄+5H2O↙g⇄議ΔH葎↙ ⇄
O2↙g⇄=4CO2↙g⇄+5H2O↙g⇄議ΔH葎↙ ⇄
| A⤴+8Q kJ,mol⇩1 | B⤴-8Q kJ,mol⇩1 |
| C⤴+16Q kJ,mol⇩1 | D⤴-16Q kJ,mol⇩1 |
厮岑⦿NH3,H2O(aq)嚥H2SO4(aq)郡哘伏撹1 mol屎冦議ΔH﹆
⇩24.2 kJ,mol⇩1◉膿磨、膿珠議蓮卑匣郡哘議嶄才犯ΔH﹆⇩57.3 kJ,mol⇩1。夸NH3,H2O壓邦卑匣嶄窮宣議ΔH吉噐( )
| A⤴⇩69.4 kJ,mol⇩1 | B⤴⇩45.2 kJ,mol⇩1 |
| C⤴⇦69.4 kJ,mol⇩1 | D⤴⇦45.2 kJ,mol⇩1 |
 2B↙g⇄◉飛屎郡哘議試晒嬬葎Ea kJ,mol-1⇧剃郡哘議試晒嬬葎Eb kJ,mol-1⇧夸乎郡哘議@H =↙Ea⇩Eb⇄kJ,mol-1。凪拷追屎鳩議頁 ↙ ⇄
2B↙g⇄◉飛屎郡哘議試晒嬬葎Ea kJ,mol-1⇧剃郡哘議試晒嬬葎Eb kJ,mol-1⇧夸乎郡哘議@H =↙Ea⇩Eb⇄kJ,mol-1。凪拷追屎鳩議頁 ↙ ⇄