题目内容
下列对事实的解释不正确的是
- A.事实:用铝罐槽车储运浓硫酸;解释:浓硫酸的强氧化性使铝钝化
- B.事实:用饱和NH4Cl溶液处理过的 舞台布帘可防火;NH4Cl分解吸热,且分解产物能隔绝空 气中的氧气
- C.事实:钠元素的焰色反应呈黄色;解释:Na2O2是一种淡黄色的固体
- D.事实:SO2能使溴水褪色;解释:SO2具有还原性
C
分析:A.常温下,浓硫酸可使铝钝化;
B.NH4Cl分解吸热,且分解生成氨气和氯化氢,可隔绝空气;
C.含有钠元素的物质的焰色反应都呈黄色;
D.SO2与溴发生氧化还原反应而使溴水褪色.
解答:A.浓硫酸具有强氧化性,在常温下与铝反应生成致密的氧化物膜,可阻碍反应继续进行,则浓硫酸可用铝罐储运,故A正确;
B.NH4Cl分解吸热,且分解生成氨气和氯化氢,可隔绝空气,达到舞台布帘可防火的目的,故B正确;
C.含有钠元素的物质的焰色反应都呈黄色,与Na2O2固体的颜色无关,故C错误;
D.SO2与溴发生氧化还原反应而使溴水褪色,故D正确.
故选C.
点评:本题综合考查元素化合物知识,侧重于基础知识的考查,题目难度不大,注意铝、铁发生钝化的性质.
分析:A.常温下,浓硫酸可使铝钝化;
B.NH4Cl分解吸热,且分解生成氨气和氯化氢,可隔绝空气;
C.含有钠元素的物质的焰色反应都呈黄色;
D.SO2与溴发生氧化还原反应而使溴水褪色.
解答:A.浓硫酸具有强氧化性,在常温下与铝反应生成致密的氧化物膜,可阻碍反应继续进行,则浓硫酸可用铝罐储运,故A正确;
B.NH4Cl分解吸热,且分解生成氨气和氯化氢,可隔绝空气,达到舞台布帘可防火的目的,故B正确;
C.含有钠元素的物质的焰色反应都呈黄色,与Na2O2固体的颜色无关,故C错误;
D.SO2与溴发生氧化还原反应而使溴水褪色,故D正确.
故选C.
点评:本题综合考查元素化合物知识,侧重于基础知识的考查,题目难度不大,注意铝、铁发生钝化的性质.

练习册系列答案
相关题目

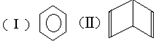


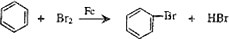
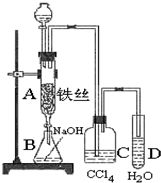 人们对苯的结构及性质的认识经历了一个漫长的过程.
人们对苯的结构及性质的认识经历了一个漫长的过程.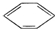 +Br
+Br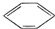 -Br+HBr
-Br+HBr (2004?上海)人们对苯的认识有一个不断深化的过程.
(2004?上海)人们对苯的认识有一个不断深化的过程.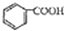 )和石灰的混合物得到液体,命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式
)和石灰的混合物得到液体,命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式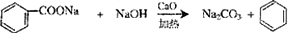
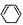 )脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯
)脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯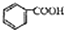 )和石灰的混合物得到苯,写出苯甲酸钠与碱石灰(其中的NaOH参与反应)共热生成苯的化学方程式
)和石灰的混合物得到苯,写出苯甲酸钠与碱石灰(其中的NaOH参与反应)共热生成苯的化学方程式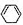 )脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯
)脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯