题目内容
6.室温下,在pH=12的NaCN溶液中,由水电离的c(OH-)为10-2 mol•L-1.分析 NaCN是强碱弱酸盐,溶液中的所有氢离子和氢氧根均来自于水的电离,但由于CN-的水解,氢离子被结合走一部分,据此分析.
解答 解:pH=12的NaCN溶液中,c(H+)=10-12mol/L,c(OH-)=10-2mol/L,由于NaCN是强碱弱酸盐,溶液中的所有氢离子和氢氧根均来自于水的电离,但由于CN-的水解,氢离子被结合走一部分,故c(H+)=10-12mol/L是被结合剩下的,故c(OH-)=10-2mol/L才是水电离出OH-的全部,即溶液中水电离出的c(OH-)=10-2mol/L,故答案为:10-2.
点评 本题考查了水的电离及其影响,题目难度中等,明确酸碱溶液抑制了水的电离,能够水解的盐促进了水的电离为解答关键,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
14.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 常温常压下,22.4L氧气所含的原子数为2NA | |
| B. | 17g的OH-离子中含有的电子数为9NA | |
| C. | 常温常压下,44gCO2含有的氧原子数为2NA | |
| D. | 标准状况下,11.2L四氯化碳所含分子数为0.5NA |
11.pH=a的某电解质溶液中,插入两只惰性电极,通直流电一段时间后,停止电解,取出电极,将溶液摇匀,测得溶液的pH>a,则该电解质溶液是( )
| A. | K2SO4 | B. | NaOH | C. | NaCl | D. | AgNO3 |
18.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 浓度均为0.1 mol•L-1的氨水和盐酸等体积混合后:c(H+)=c(OH-)+c(NH3•H2O) | |
| B. | 等浓度的碳酸钠、碳酸氢钠溶液混合后:c(CO${\;}_{3}^{2-}$)<c(HCO${\;}_{3}^{-}$) | |
| C. | 在NaHB溶液中一定有:c(Na+)=c(HB-)+2c(B2-) | |
| D. | Na2CO3溶液中:2c(Na+)=c(CO${\;}_{3}^{2-}$)+c(HCO${\;}_{3}^{-}$)+c(H2CO3) |
15.如图R、W、X、Y、Z为五种物质,若箭头表示能一步转化的常见反应,则其中常温下能实现图示转化关系的是( )
| 选项 | R | W | X | Y | Z | 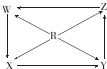 |
| A | Si | SiO2 | H2SiO2 | Na2SiO2 | SiCl4 | |
| B | Na | Na2O | Na2O2 | Na2CO3 | NaOH | |
| C | Fe | Fe(OH)2 | FeCl3 | FeCl3 | Fe(NO4)3 | |
| D | Al | NaAlO2 | Al2(SO4)3 | AlCl3 | Al(NO4)3 |
| A. | A | B. | B | C. | C | D. | D |
16.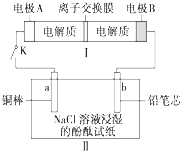 如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为NaCl和酚酞和混合溶液浸湿的滤纸,离子交换膜只允许Na+通过,电池充电、放电的化学方程式为2Na2S2+NaBr3$\frac{\underline{\;放电\;}}{充电}$Na2S4+3NaBr.闭合开关K时,b极附近先变红色.下列说法正确的是( )
如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为NaCl和酚酞和混合溶液浸湿的滤纸,离子交换膜只允许Na+通过,电池充电、放电的化学方程式为2Na2S2+NaBr3$\frac{\underline{\;放电\;}}{充电}$Na2S4+3NaBr.闭合开关K时,b极附近先变红色.下列说法正确的是( )
 如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为NaCl和酚酞和混合溶液浸湿的滤纸,离子交换膜只允许Na+通过,电池充电、放电的化学方程式为2Na2S2+NaBr3$\frac{\underline{\;放电\;}}{充电}$Na2S4+3NaBr.闭合开关K时,b极附近先变红色.下列说法正确的是( )
如图所示装置Ⅰ是一种可充电电池,装置Ⅱ为NaCl和酚酞和混合溶液浸湿的滤纸,离子交换膜只允许Na+通过,电池充电、放电的化学方程式为2Na2S2+NaBr3$\frac{\underline{\;放电\;}}{充电}$Na2S4+3NaBr.闭合开关K时,b极附近先变红色.下列说法正确的是( )| A. | 电池充电时,电极B连接直流电源的正极 | |
| B. | 电池放电过程中Na+从左到右通过离子交换膜 | |
| C. | 闭合开关K后,b电极附近pH变小 | |
| D. | 当b电极上析出气体1120mL(标准状况)时,有0.1 molNa+通过离子交换膜 |
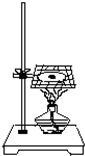 如图所示,将一小块钠放在石棉网上加热.回答下列问题:
如图所示,将一小块钠放在石棉网上加热.回答下列问题: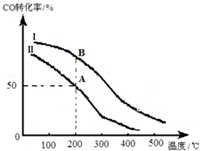 甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物.工业上可用CO和H2制取甲醇,化学方程式为:CO(g)+2H2(g)═CH3OH(g)△H=b kJ/mol,
甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物.工业上可用CO和H2制取甲醇,化学方程式为:CO(g)+2H2(g)═CH3OH(g)△H=b kJ/mol,