题目内容
常温下,向体积为10 mL、物质的量浓度均为0.1 mol/L的盐酸和醋酸的混合溶液中滴入0.1 mol/L NaOH溶液。下列说法错误的是( )
| A.加入NaOH溶液后,溶液一定满足: c(H+)+c(Na+)=c(OH-)+c(C1-)+c(CH3COO-) |
| B.加入10 mLNaOH溶液时,溶液满足(溶液体积变化忽略不计): c(CH3COO-)+c(CH3COOH)="0.05" mol/L |
| C.加入15 mLNaOH溶液时,呈酸性,溶液满足: c(Na+)>c(C1-)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) |
| D.加入足量NaOH溶液时,溶液中发生的中和反应的热化学方程式表示为: |
D
解析试题分析:A、是止确的电荷守恒表达式,与氢氧化钠溶液的体积无关;B、加入l0 mLNaOH溶液时,溶液体积增倍,根据元素守恒知,正确;C、加入15 mLNaOH溶液时,盐酸完全反应,并得到等物质的量的HAc与NaAc的混合溶液,溶液呈酸性,所以c(CHCOO-)>c(CHCOOH),正确;D、醋酸是弱酸,书写离了方程式时必须保留化学式,ΔH也错,错误。
考点:考查电解质溶液,涉及离子反应、离子浓度大小比较以及中和热相关知识。

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
已知25℃时有关弱酸的电离平衡常数:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
25℃下,下列有关说法正确的是
A.浓度为0.1mol/L的HCN溶液中c(OH-)=10-13mol/L
B.物质的量浓度相同的稀酸溶液中KW:CH3COOH>H2CO3>HCN
C.物质的量浓度相同的三种钠盐溶液的pH:NaHCO3>NaCN>CH3COONa
D.浓度均为amol?L-1HCN溶液与NaOH溶液等体积混合充分反应后的溶液中(忽略体积的变化)c(H+)<c(OH-)<c(CN-)<0.5amol/L
SO2的烟气会形成酸雨,工业上常利用Na2SO3溶液作为吸收液脱除烟气中的SO2。随着SO2的吸收,吸收液的pH不断变化。下列粒子浓度关系一定正确的是
| A.Na2SO3溶液中存在:c(Na+)>c(SO32-)>c(H2SO3)>c(HSO3-) |
| B.已知NaHSO3溶液pH<7,该溶液中:c(Na+)>c(HSO3-)>c(H2SO3) >c(SO32-) |
| C.当吸收液呈中性时:c(Na+)=2 c(SO32-)+c(HSO3-) |
| D.当吸收液呈酸性时:c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) |
水的电离平衡曲线如图所示。下列说法错误的是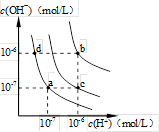
| A.水的电离常数KW数值大小关系为:b>c>d |
| B.a点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42- |
| C.温度不变,加入少量NaOH可使溶液从c点变到 a点 |
| D.在b点对应温度下,将pH=2的HCl与pH=10的NaOH溶液等体积混合后,溶液显中性 |
20℃时向20mL 0.1mol·L-1醋酸溶液中不断滴入0.1mol·L-1NaOH(aq),溶液pH变化如图所示。此过程里溶液中离子浓度的关系错误的是 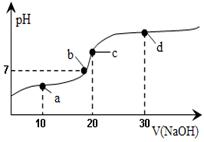
| A.a点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.b点:c(Na+) = c(CH3COO-)>c(H+) = c(OH-) |
| C.c点:c(H+) = c(CH3COOH) + c(OH-) |
| D.d点:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
下列各溶液中,微粒的物质的量浓度关系表述正确的是
| A.0.1 mol/LNa2CO3溶液中:c(Na+)=(HCO3-)+c(H2CO3)+2c(CO32-) |
| B.常温下pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7 |
| C.将0.2mol/LNaA溶液和0.1 mol·L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) |
| D.pH=l2的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等 |
25℃时,下列各项分别由等体积0.1 mol·L-1的两种溶液混合,有关混合后的溶液说法不正确的是( )
| A.Ba(OH)2溶液与Na2SO4溶液:pH="13" |
| B.醋酸与CH3COONa溶液:c(Na+)+c(H+)= c(CH3COO-)+c(OH-) |
| C.Na2CO3溶液与NaHCO3溶液:2c(Na+) = 3c(CO32-)+3c(HCO3-)+3c(H2CO3) |
| D.Na2CO3溶液与NaOH溶液: c(Na+)>c(CO32-)>c(OH-)>c(H+) |
