题目内容
【题目】在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物 质 | X | Y | Z |
初始浓度/ mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/ mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A. 反应达到平衡时,X的转化率为50%
B. 增大压强,使平衡向生成Z的方向移动,平衡常数增大
C. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
D. 改变温度可以改变此反应的平衡常数
【答案】B
【解析】A.反应达到平衡时,X的转化率为: ![]() =50%,故A正确;B.增大压强,使平衡向生成Z的方向移动,但温度不变,平衡常数不变,故B错误;C.根据反应速率之比等于浓度变化量之比等于化学计量数之比可知:△c(X)∶△c(Y)∶△c(Z)=0.05∶0.15∶0.1=1∶3∶2,则反应的方程式为X+3Y2Z,K=
=50%,故A正确;B.增大压强,使平衡向生成Z的方向移动,但温度不变,平衡常数不变,故B错误;C.根据反应速率之比等于浓度变化量之比等于化学计量数之比可知:△c(X)∶△c(Y)∶△c(Z)=0.05∶0.15∶0.1=1∶3∶2,则反应的方程式为X+3Y2Z,K=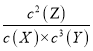 =
=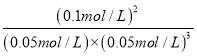 =1600(mol/L)-2,故C正确;D.平衡常数只受温度的影响,温度改变时,化学平衡常数一定变化,故D正确;答案为B。
=1600(mol/L)-2,故C正确;D.平衡常数只受温度的影响,温度改变时,化学平衡常数一定变化,故D正确;答案为B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】实验室里用下列仪器和药品制取纯净的无水氯化铜.根据要求完成以下问题:
序号 | ① | ② | ③ | ④ | ③ | ⑥ |
仪器及装置图 |
|
|
|
|
|
|
(1)按气体从左向右流动,装置②在④左边,则②中加入的液体是;
(2)装置⑤中发生反应的化学方程式是;
(3)实验开始时,应先点燃(填装置序号)处的酒精灯,否则CuCl2中含有(填化学式)杂质.待充分反应后,装置①的玻璃管中剩余物呈色;
(4)某实验小组组装装置时,在①和⑥之间添加了一个盛有浓硫酸的洗气瓶,其作用是 .