题目内容
将SO2通入CuSO4和NaCl的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀分析,知其中含Cl:35.7%,Cu:64.3%,SO2在上述反应中作用是
| A.酸 | B.漂白剂 | C.氧化剂 | D.还原剂 |
D
该反应的方程式为:
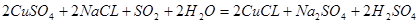 ;即SO2在上述反应中作用是还原剂作用;
;即SO2在上述反应中作用是还原剂作用;
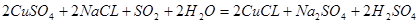 ;即SO2在上述反应中作用是还原剂作用;
;即SO2在上述反应中作用是还原剂作用;
练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
题目内容
| A.酸 | B.漂白剂 | C.氧化剂 | D.还原剂 |
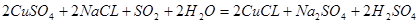 ;即SO2在上述反应中作用是还原剂作用;
;即SO2在上述反应中作用是还原剂作用;
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案