题目内容
(14分)向某密闭容器中加入0.6molA、0.2molC和一定量的B三种气体,一定条件下发生反应,各物质浓度随时间变化如甲图所示(其中t0-t1阶段c(B)未画出)。乙图为反应体系中反应速率随时间变化的情况,且四个阶段都只改变一种条件(催化剂、温度、浓度、压强,每次改变条件均不同),已知t3~t4阶段为使用催化剂。
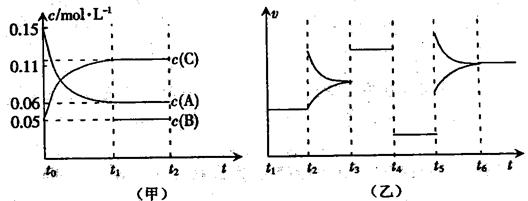
(1)若t1=5s,则t0~t1阶段以C浓度变化表示的反应速率为v(C)=________mol/(L?s)。
(2)若t2~t3阶段,C的体积分数变小,此阶段v(正)___v(逆)(填“>”、“=”或“<”)。
(3)t4~t5阶段改变的条件为_______,B的起始物质的量为_______。
(4)t5~t6阶段容器内A的物质的量共减小0.03mol,而此过程中容器与外界的热交换总量为akJ,写出该反应的热化学方程式:__________________________________。
(5)该反应的化学平衡常数K可表示为_______________。[用含c(A) 、c(B) 、c(C)的式子表示]
并在下图中补画出t1~t6 各阶段K的变化趋势图像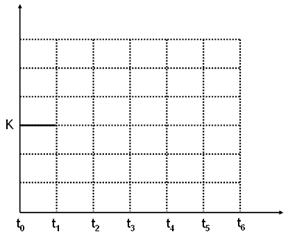

(1)若t1=5s,则t0~t1阶段以C浓度变化表示的反应速率为v(C)=________mol/(L?s)。
(2)若t2~t3阶段,C的体积分数变小,此阶段v(正)___v(逆)(填“>”、“=”或“<”)。
(3)t4~t5阶段改变的条件为_______,B的起始物质的量为_______。
(4)t5~t6阶段容器内A的物质的量共减小0.03mol,而此过程中容器与外界的热交换总量为akJ,写出该反应的热化学方程式:__________________________________。
(5)该反应的化学平衡常数K可表示为_______________。[用含c(A) 、c(B) 、c(C)的式子表示]
并在下图中补画出t1~t6 各阶段K的变化趋势图像

(1)0.012 (2分) (2)<(2分)
(3)减压(或增大容器体积)(2分) 0.08mol(2分)
(4)3A(g) B(g)+2C(g);△H="+100a" kJ/mol(2分)
B(g)+2C(g);△H="+100a" kJ/mol(2分)
(5)K=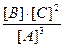 (与图像各2分)
(与图像各2分)

(3)减压(或增大容器体积)(2分) 0.08mol(2分)
(4)3A(g)
 B(g)+2C(g);△H="+100a" kJ/mol(2分)
B(g)+2C(g);△H="+100a" kJ/mol(2分)(5)K=
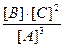 (与图像各2分)
(与图像各2分)
略

练习册系列答案
相关题目
 C(g)+D(g)
C(g)+D(g)
 bZ(g);△H<0。如图是容器中X、Z的物质的量浓度随时间变化的曲线。下列说法正确的是( )
bZ(g);△H<0。如图是容器中X、Z的物质的量浓度随时间变化的曲线。下列说法正确的是( )
 0~10min容器内气体的压强逐渐增大
0~10min容器内气体的压强逐渐增大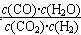 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
 N2O4
N2O4 2C(g);△H < 0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2 kJ,已知Q1=3Q2。下列叙述错误的是( )
2C(g);△H < 0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2 kJ,已知Q1=3Q2。下列叙述错误的是( ) 图中表示外界条件(t、p)的变化对下列可逆反应的影响:
图中表示外界条件(t、p)的变化对下列可逆反应的影响: 2R(g);△H>0,y 轴表示的是 ( )
2R(g);△H>0,y 轴表示的是 ( )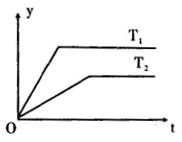
 2SO2(g)+O2(g)2SO3(g)△H=一196.6 kJ·mol-1。
2SO2(g)+O2(g)2SO3(g)△H=一196.6 kJ·mol-1。