题目内容
17.为了延长果实或花朵的成熟期,可用在某液体中浸泡过的硅土来吸收水果或花朵产生的乙烯,以达到上述目的.则这种液体可能是( )| A. | 水 | B. | 浓盐酸 | C. | 高锰酸钾溶液 | D. | 苯 |
分析 乙烯是植物激素,能催熟果实或花朵,如要延长果实或花朵的成熟期,应用物质来吸收乙烯,即选用的溶液必须能吸收乙烯,据此分析.
解答 解:乙烯是植物激素,能催熟果实或花朵,如要延长果实或花朵的成熟期,应用物质来吸收乙烯,即选用的溶液必须能吸收乙烯.
A、乙烯不溶于水,故A错误;
B、乙烯和浓盐酸不反应,故B错误;
C、乙烯能被高锰酸钾溶液氧化从而被吸收,故C正确;
D、苯虽然能溶解乙烯,但苯有毒,故不适合用于来吸收水果或花朵产生的乙烯,故D错误.
故选C.
点评 本题借助延缓果实和花朵的催熟这个问题来考查了乙烯的性质,应注意的是乙烯中的官能团为碳碳双键,比较脆弱,易被氧化和加成.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
7.用如图所示NaClO的发生装置对海水进行消毒和灭藻处理,有关说法不正确的是( )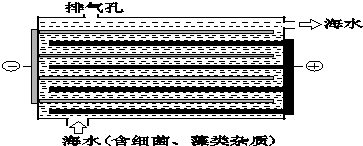

| A. | 海水淡化前需进行预处理,通常用明矾[K2SO4•Al2(SO4)3•24H2O]作混凝剂,降低浊度,明矾水解的离子方程式是:Al3++3H2O?Al(OH)3+3H+ | |
| B. | 装置中由NaCl转化为NaClO的化学方程式是:NaCl+H2O═H2↑+NaClO | |
| C. | 海水中含有Ca2+、Mg2+、HCO3-等杂质离子,处理过程中装置的阴极易产生水垢,其主要成分是Mg(OH)2和CaCO3 | |
| D. | 若每隔5-10 min倒换一次电极电性,可有效地解决阴极的结垢问题 |
8.四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题.
(1)W元素和氢可形成离子化合物,其电子式为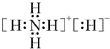 .
.
(2)Y元素和Z元素可形成YZ3化合物,可用于净水剂,净水原理Al3++3H2O=Al(OH)3(胶体)+3H+(用离子方程式表示).
(3)①下列可作为比较X和Y金属性强弱的依据是abc (填序号).
a.最高价氧化物的水化物能反应 b.相应硫酸盐水溶液的pH
c.单质与水反应的难易程度 d.单质与酸反应时失去的电子数
②由X、Y、氢、氧四种元素所组成的化合物,能与盐酸以1:4反应生成两种常见盐和水,则该化合物的化学式为NaAl(OH)4.
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似.体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,混合后溶液中离子浓度由大到小的顺序是c(Na+)>c(N3-)>c(OH-)>c(H+).
| W | X | Y | Z | |
| 结构 或性质 | 最高价氧化物对应的水 化物与其气态氢化物反 应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最 低负价之和为6 |
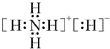 .
.(2)Y元素和Z元素可形成YZ3化合物,可用于净水剂,净水原理Al3++3H2O=Al(OH)3(胶体)+3H+(用离子方程式表示).
(3)①下列可作为比较X和Y金属性强弱的依据是abc (填序号).
a.最高价氧化物的水化物能反应 b.相应硫酸盐水溶液的pH
c.单质与水反应的难易程度 d.单质与酸反应时失去的电子数
②由X、Y、氢、氧四种元素所组成的化合物,能与盐酸以1:4反应生成两种常见盐和水,则该化合物的化学式为NaAl(OH)4.
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似.体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,混合后溶液中离子浓度由大到小的顺序是c(Na+)>c(N3-)>c(OH-)>c(H+).
9.下列实验的现象、解释或结论正确的是( )
| 实验 | 解释或结论 | |
| A | 向某溶液中持续通入CO2,先出现白色胶状沉淀,通至过量,沉淀不溶解,证明存在[Al(OH)4] | Al(OH)3不溶于碳酸 |
| B | 将SO2通入紫色高锰酸钾溶液中,溶液褪色 | SO2具有还原性 |
| C | 用蒸馏法将溶解在CCl4中的碘分离出来 | 碘易升华,先分离出 |
| D | 向Fe(NO3)2溶液滴入硫酸酸化的H2O2溶液,溶液变黄色 | 氧化性:H2O2>Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
6.以下实验能获得成功的是( )
| A. | 把银氨溶液和少量乙醛加入试管中再酒精灯上加热制银镜 | |
| B. | 将铁屑、溴水、苯混合制溴苯 | |
| C. | 在苯酚溶液中滴入少量稀溴水出现白色沉淀 | |
| D. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
 的流程(无机试剂任用).有机合成流程示例如下:
的流程(无机试剂任用).有机合成流程示例如下: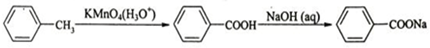
 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
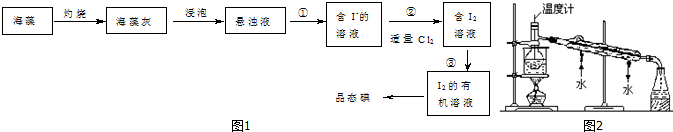 (1)指出提取的过程中有关实验操作名称:①过滤;③萃取、分液;
(1)指出提取的过程中有关实验操作名称:①过滤;③萃取、分液;