题目内容
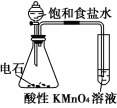
【题目】某校化学兴趣小组根据反应 H2O2+2HI=2H2O+I2 探究影响化学反应速率的因素。实验数据如下
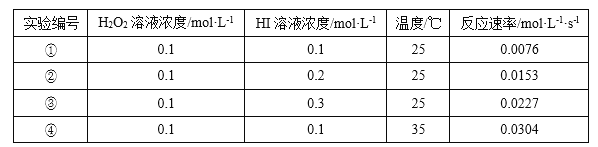
回答下列问题:
(1)反应 H2O2+2HI=2H2O+I2 中,氧化剂是_____。
(2)25℃时,表明增大反应物浓度,化学反应速率_____(填“增大”成“减小”)。
(3)能表明温度对化学反应速率影响的实验编号是①和_____。
(4)H2O2 不稳定,写出 H2O2 发生分解反应的化学方程式:_____。
【答案】H2O2 增大 ④ 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
【解析】
(1)得到电子化合价降低的是氧化剂;
(2)根据浓度对反应速率的影响分析解答;
(3)探究温度对反应速率的影响,其它条件不变;
(4)双氧水分解生成氧气和水,据此书写。
(1)反应H2O2+2HI=2H2O+I2中氧元素化合价降低,得到电子发生还原反应,氧化剂是H2O2。
(2)根据表中数据可知25℃时,增大反应物浓度,化学反应速率增大。
(3)要探究温度对反应速率的影响,其它条件不变,因此根据表中数据可知能表明温度对化学反应速率影响的实验编号是①和④。
(4)H2O2不稳定易分解生成氧气和水,则H2O2发生分解反应的化学方程式为2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。

【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
熔点/℃ | 85.5 | 115.2 | >600(分解) | 75.5 | 16.8 | 10.3 |
沸点/℃ | 60.3 | 444.6 | 10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为__________,基态S原子电子占据最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________。

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为_____形,其中共价键的类型有______种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm3;晶胞中Fe2+位于![]() 所形成的正八面体的体心,该正八面体的边长为______nm。
所形成的正八面体的体心,该正八面体的边长为______nm。
【题目】下述实验方案中均使用了NaCl溶液,能达到实验目的的是( )
编号 | A | B | C | D |
实验 方案 |
置于光亮处 |
|
片刻后在Fe电极附近滴入K3[Fe(CN)6]溶液 |
|
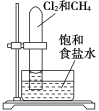
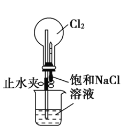
实验 目的 | 验证甲烷与氯气发生化学反应 | 进行喷泉实验 | 验证Fe电极被保护 | 验证乙炔的还原性 |
A.AB.BC.CD.D