题目内容
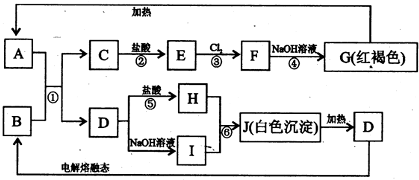
下列A-J均是中学化学中常见物质,A、B、C、E、H是常见 气体,E气体可用固态的D干燥,①、②是工业生产中的重要反应,它们的部分关系如图所示:
气体,E气体可用固态的D干燥,①、②是工业生产中的重要反应,它们的部分关系如图所示:
试回答下列问题:
(1)I的化学式为:
(2)反应①的离子方程式:
(3)B与足量的E可生成I及另一种常见单质,写出该反应的化学方程式,并标明电子转移方向和数目:
 .
.
(4)为保证反应②的顺利进行,并得到足够量的J,应采取的措施是(写出其中两条):①
 气体,E气体可用固态的D干燥,①、②是工业生产中的重要反应,它们的部分关系如图所示:
气体,E气体可用固态的D干燥,①、②是工业生产中的重要反应,它们的部分关系如图所示:试回答下列问题:
(1)I的化学式为:
NH4Cl
NH4Cl
.(2)反应①的离子方程式:
2Cl-+2H2O
2OH-+H2↑+Cl2↑
| ||
2Cl-+2H2O
2OH-+H2↑+Cl2↑
.
| ||
(3)B与足量的E可生成I及另一种常见单质,写出该反应的化学方程式,并标明电子转移方向和数目:


(4)为保证反应②的顺利进行,并得到足够量的J,应采取的措施是(写出其中两条):①
氯化钠溶液必须饱和
氯化钠溶液必须饱和
②在食盐水中先通氨气至饱和再通入足量的二氧化碳气体
在食盐水中先通氨气至饱和再通入足量的二氧化碳气体
.分析:A、B、C、E、H是常见气体,E气体可用固态的D干燥,则E应为NH3,①、②是工业生产中的重要反应,结合(3)可知,B为Cl2,C为H2,A为HCl,则E与A反应生成I为NH4Cl,H为CO2,F、G其中一种为H2O,一种为NaCl,D为NaOH,J为NaHCO3,即反应①为氯碱工业的反应,反应②为制碱工业,然后结合物质的性质来解答.
解答:解:A、B、C、E、H是常见气体,E气体可用固态的D干燥,则E应为NH3,①、②是工业生产中的重要反应,结合(3)可知,B为Cl2,C为H2,A为HCl,则E与A反应生成I为NH4Cl,H为CO2,F、G其中一种为H2O,一种为NaCl,D为NaOH,J为NaHCO3,即反应①为氯碱工业的反应,反应②为制碱工业,
(1)由上述分析可知,I为NH4Cl,故答案为:NH4Cl;
(2)反应①的离子反应为2Cl-+2H2O
2OH-+H2↑+Cl2↑,故答案为:2Cl-+2H2O
2OH-+H2↑+Cl2↑;
(3)氨气与氯气反应生成氮气和氯化铵,该反应及转移电子数为 ,
,
故答案为: ;
;
(4)保证反应②的顺利进行,并得到足够量的J,采取措施为①氯化钠溶液必须饱和,②在食盐水中先通氨气至饱和再通入足量的二氧化碳气体,
故答案为:氯化钠溶液必须饱和;在食盐水中先通氨气至饱和再通入足量的二氧化碳气体.
(1)由上述分析可知,I为NH4Cl,故答案为:NH4Cl;
(2)反应①的离子反应为2Cl-+2H2O
| ||
| ||
(3)氨气与氯气反应生成氮气和氯化铵,该反应及转移电子数为
 ,
,故答案为:
 ;
;(4)保证反应②的顺利进行,并得到足够量的J,采取措施为①氯化钠溶液必须饱和,②在食盐水中先通氨气至饱和再通入足量的二氧化碳气体,
故答案为:氯化钠溶液必须饱和;在食盐水中先通氨气至饱和再通入足量的二氧化碳气体.
点评:本题考查无机物的推断,物质的推断是解答本题的关键,注意两个工业反应为解答本题的突破口,题目难度中等.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
(8分)、下列A~K是中学化学中的常见物质,其中D、E、K为单质,其余物质为化合物。这些物质具有下列转化关系(省略了水和部分反应物及生成物),除反应②外,其他反应均在溶液中进行。D是工业中最常用的金属。
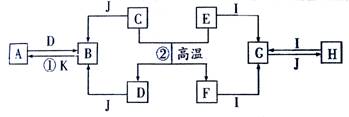
(1)A、H分别为 、 (填化学式)
(2)写出反应②的化学方程式 。
(3)2.7克E与I完全反应生成G,G与J反应生成3.9克H ,则消耗J的物质的量为 。
(4)实验指出,无水H在常压条件下不同温度时的密度为:
|
T(℃) |
200 |
600 |
800 |
|
ρ(g/L) |
6.881 |
2.650 |
1.517 |
|
气体摩尔体积(L/mol) |
38.8 |
71.6 |
88.0 |
可见,600℃时无水H 存在形式的分子式为 。

 气体,E气体可用固态的D干燥,①、②是工业生产中的重要反应,它们的部分关系如图所示:
气体,E气体可用固态的D干燥,①、②是工业生产中的重要反应,它们的部分关系如图所示: