题目内容
7.升高温度,下列数据不一定增大的是( )| A. | 化学反应速率? | B. | 反应物平衡转化率α | ||
| C. | 水的离子积常数Kw | D. | 盐的水解平衡常数Kh |
分析 A、升高温度活化分子数目增大,有效碰撞次数增多,反应速率一定加快.这一点不要和化学平衡的移动混淆;
B、根据勒夏特列原理,对所有可逆反应升温平衡都向吸热的方向移动.可逆反应的正反应既有吸热反应也有放热反应,要区别对待;
C、水的电离过程是吸热的,升高温度促进水的电离;
D、盐类水解是吸热反应.
解答 解:A、升高温度活化分子数目增大,有效碰撞次数增多,反应速率一定加快,故A不选;
B、若正反应为放热反应,升高温度平衡向逆反应移动,反应物转化率减小,若正反应为吸热反应,升高温度平衡向正反应移动,反应物转化率增大,故B选;
C、水的电离过程是吸热的,升高温度促进水的电离,升高温度电离程度增大,水的离子积一定增大,故C不选;
D、升温促进盐类水解,盐的水解平衡常数Kh增大,故D不选.
故选B.
点评 本题考查温度对水的离子积、电离平衡常数、反应速率以及化学平衡常数的影响,比较基础.注意温度对化学反应速率和化学平衡影响的区别,不要混淆.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
18.下列化学方程式中,不可以用H++OH-=H2O表示的是( )
| A. | Cu(OH)2+2HNO3═Cu(NO3)2+2H2O | B. | Ba(OH)2+2HCl═BaCl2+2H2O | ||
| C. | 2NaOH+H2SO4═Na2SO4+2H2O | D. | KOH+HCl═KCl+H2O |
12.一定条件下,在一恒容密闭容器中,能表示反应 X(s)+2Y(g)?2Z(g) 一定达到化学平衡状态的是( )
①单位时间内生成2n mol Z,同时消耗2n mol Y ②X的质量不再发生变化
③容器中的压强不再发生变化 ④容器中气体的密度不再发生变化.
①单位时间内生成2n mol Z,同时消耗2n mol Y ②X的质量不再发生变化
③容器中的压强不再发生变化 ④容器中气体的密度不再发生变化.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
19.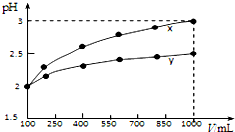 有100mL pH=2的两种一元酸x和y,稀释过程中溶液pH与体积的关系如图所示,则下列有关说法中正确的是( )
有100mL pH=2的两种一元酸x和y,稀释过程中溶液pH与体积的关系如图所示,则下列有关说法中正确的是( )
 有100mL pH=2的两种一元酸x和y,稀释过程中溶液pH与体积的关系如图所示,则下列有关说法中正确的是( )
有100mL pH=2的两种一元酸x和y,稀释过程中溶液pH与体积的关系如图所示,则下列有关说法中正确的是( )| A. | 稀释前x、y的物质的量浓度相等 | B. | 相同温度下,电离常数Ka(x)>Ka(y) | ||
| C. | 随着稀释的进行,y的电离程度减小 | D. | 稀释相同倍数后的溶液中c(H+):x>y |
16.下列反应中,生成的有机物只有一种是( )
| A. | 甲烷和氯气混合光照 | B. | 苯酚与溴水反应 | ||
| C. | 丙烯和氯化氢发生加成反应 | D. | 1-丁烯和氢气发生加成反应 |

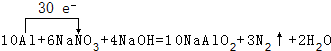 .
.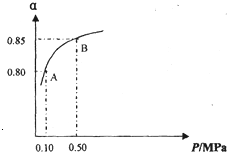 二氧化硫和氮的氧化物是常用的工业原料,但也是大气的主要污染物.综合治理基污染是环境化学当前的重要研究内容之一.
二氧化硫和氮的氧化物是常用的工业原料,但也是大气的主要污染物.综合治理基污染是环境化学当前的重要研究内容之一.