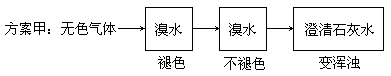
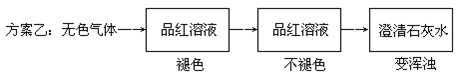
题目内容
某研究小组利用下图装置探究温度对CO还原Fe2O3的影响(固定装置略)

(1)MgCO3的分解产物为 。
(2)装置C的作用是 ,处理尾气的方法为 。
(3)将研究小组分为两组,按图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。
①乙组得到的黑色粉末是 ;
②甲组步骤1中反应的离子方程式为 ;
③乙组步骤4中,溶液变红的原因为 ;溶液褪色可能的原因及其验证方法为 ;
④从实验安全考虑,题9图装置还可采取的改进措施是 。

(1)MgCO3的分解产物为 。
(2)装置C的作用是 ,处理尾气的方法为 。
(3)将研究小组分为两组,按图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
①乙组得到的黑色粉末是 ;
②甲组步骤1中反应的离子方程式为 ;
③乙组步骤4中,溶液变红的原因为 ;溶液褪色可能的原因及其验证方法为 ;
④从实验安全考虑,题9图装置还可采取的改进措施是 。
(15分)
(1)MgO、CO2
(2)除CO2,点燃
(3)①Fe
②Fe3O4+8H+=2Fe3++Fe2++4H2O
③Fe2+被氧化为Fe3+,Fe3+遇SCN?显红色;假设SCN?被Cl2氧化,向溶液中加入KSCN溶液,若出现红色,则假设成立(其它合理答案均可得分)
④在装置BC之间添加装置E防倒吸(其它合理答案均可得分)
(1)MgO、CO2
(2)除CO2,点燃
(3)①Fe
②Fe3O4+8H+=2Fe3++Fe2++4H2O
③Fe2+被氧化为Fe3+,Fe3+遇SCN?显红色;假设SCN?被Cl2氧化,向溶液中加入KSCN溶液,若出现红色,则假设成立(其它合理答案均可得分)
④在装置BC之间添加装置E防倒吸(其它合理答案均可得分)
(1)类比CaCO3的煅烧分解,可推知MgCO3分解生成MgO和CO2
(2)因为后面要通过F检验CO与Fe2O3反应的产物CO2,所以装置C除去CO中的CO2;尾气中含有有毒气体CO,采用点燃的方法可除去CO。
(3)①分析乙组现象,乙与盐酸反应产生气体,为Fe。
②分析甲组现象,可知甲组反应后含有+2价铁和+3价铁,为Fe3O4,与盐酸反应生成Fe3+、Fe3+和H2O,配平既得方程式。
③因为步骤4加入了新制氯水,能把Fe2+氧化为Fe3+,遇SCN?变红:新制氯水具有强氧化性,所以溶液褪色的原因可能是:新制氯水氧化了SCN?,检验方法是再加入KSCN溶液,若出现红色,说明原来的SCN?被氧化,假设成立。
④因为CO2易与NaOH反应,直接用导管通入可能发生倒吸,所以在装置BC之间添加防倒吸装置。
【考点定位】本题考查实验装置、实验方法、实验现象、产物的判断以及方程式的书写。

练习册系列答案
相关题目
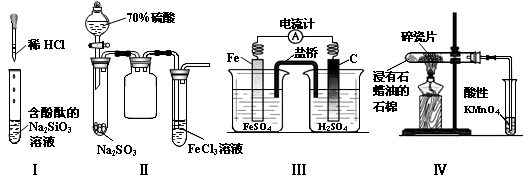
 CuO + SO3↑ 2SO3
CuO + SO3↑ 2SO3  2SO2↑+ O2↑
2SO2↑+ O2↑
 2SO2(g) + O2(g)的平衡常数表达式为K= 。
2SO2(g) + O2(g)的平衡常数表达式为K= 。