题目内容
【题目】I.下面是石蜡油在炽热碎瓷片的作用下产生乙烯并检验乙烯性质的实验。请回答下列问题:
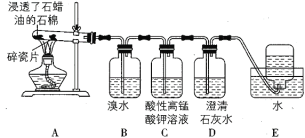
(1)A中碎瓷片的作用是____________
(2)B装置中反应的化学方程式为_______
(3)C装置中可观察到的现象是_____________
(4)D中的现象是_______________
(5)除去甲烷中乙烯的方法是将气体依次通过盛有____、浓硫酸的洗气瓶。
a 酸性高锰酸钾溶液 b 水 c 溴水 d 氢氧化钠溶液
【答案】催化剂 CH2=CH2 + Br2 → CH2Br-CH2Br 溶液褪色 澄清石灰水变浑浊 c
【解析】
石蜡油在炽热碎瓷片做催化剂的作用下产生乙烯,将生成的气体通入溴水,若溴水褪色,说明乙烯具有不饱和性,含有碳碳双键,将B中出来的气体通入酸性高锰酸钾溶液中,高锰酸钾具有氧化性,可以观察到高锰酸钾溶液褪色,生成的气体在通过澄清石灰水,石灰水变浑浊,说明从C中出来的气体中含有二氧化碳,即乙烯被高锰酸钾溶液氧化为二氧化碳,说明乙烯具有还原性,据此分析解答。
(1)石蜡油需要在催化剂的作用下能发生分解反应,A中碎瓷片的作用催化作用;
(2)B装置中乙烯和溴水发生加成反应生成1,2-二溴乙烷,反应的化学方程式为CH2=CH2 + Br2 →CH2Br-CH2Br;
(3)石蜡油生成的乙烯能被酸性高锰酸钾溶液氧化,所以C装置中可观察到的现象是溶液紫(或紫红)色褪去;
(4)乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能使澄清石灰水变浑浊,D中的现象是澄清石灰水变浑浊;
(5)a.甲烷与酸性高锰酸钾溶液不反应、乙烯被酸性高锰酸钾氧化为二氧化碳气体,引入新杂质,故a不符合题意;
b.甲烷、乙烯都不溶于水,也不与水反应,故b不符合题意;
c.甲烷与溴水不反应、乙烯与溴水发生加成反应生成1,2-二溴乙烷,且使溴水褪色,故c符合题意;
d.甲烷、乙烯都不与氢氧化钠溶液反应,不能除去乙烯,故d不符合题意;
答案选c。