题目内容
【题目】氮及其化合物与生产生活关系密切。请完成下列填空:
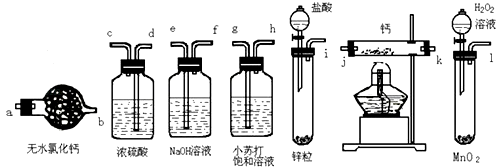
(1)某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。

①装置甲中盛放浓硝酸的仪器A的名称是__________________, 装置丙中的试管内发生反应的离子方程式为:______________________________。
②实验过程中装置乙、丙中出现的现象分别是________________________;______________。
(2)NO在医疗上有重要的应用,曾被科学家作为研究的重要物质。现有容积为aL的试管盛满NO后倒扣于水槽中,再向试管中通入一定体积O2后,试管内气体的体积为试管容积的一半,则通入的O2的在相同条件下体积为____________。
A.0.75aL B.0.375aL C.0.625aL D.1.25aL
(3)在盛有一定量浓硝酸的试管中加入12.8g的铜片发生反应。请回答下列问题:
①开始阶段,反应的化学方程式为_______________________________,后一阶段生成的气体为
_______,若两者恰好完全反应整个反应过程共产生标准状况下气体2.24L,则反应过程中被还原的HNO3的物质的量为__________ mol.,参加反应的HNO3的物质的量为__________ mol.。
②反应结束后往试管中加入铜片,再加入少量20%的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式为____________________________________________________。
【答案】 分液漏斗 3NO2+H2O = 2H++2NO+NO 产生红棕色气体 蒸馏水中有气泡,生成无色气体 BD Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O NO 0.1mol 0.5mol 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
【解析】(1)①根据仪器A的结构特点知,A为分液漏斗;装置丙中的试管内二氧化氮与水反应生成硝酸和一氧化氮,发生反应的离子方程式为:3NO2+H2O = 2H++2NO+NO;②实验过程中装置乙、丙中出现的现象分别是产生红棕色气体、蒸馏水中有气泡,生成无色气体;(2)根据反应4NO+3O2+2H2O===4HNO3,若反应后试管中剩余的是氧气,则参与反应的氧气的体积为![]() ,则通入的O2的在相同条件下体积为
,则通入的O2的在相同条件下体积为![]() ;若反应后试管中剩余的是NO,则通入的O2的在相同条件下体积为
;若反应后试管中剩余的是NO,则通入的O2的在相同条件下体积为![]() ;答案选BD;(3)①开始阶段,铜与浓硝酸反应产生二氧化氮,反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2 +2NO2↑+2H2O,随着反应的进行,浓硝酸变为稀硝酸,稀硝酸与铜反应,后一阶段生成的气体为NO,若两者恰好完全反应整个反应过程共产生标准状况下气体2.24L,即0.1molNO2和NO气体,根据氮原子守恒,则反应过程中被还原的HNO3的物质的量为0.1mol,反应后生成的Cu(NO)3中含有NO3-的物质的量为2×
;答案选BD;(3)①开始阶段,铜与浓硝酸反应产生二氧化氮,反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2 +2NO2↑+2H2O,随着反应的进行,浓硝酸变为稀硝酸,稀硝酸与铜反应,后一阶段生成的气体为NO,若两者恰好完全反应整个反应过程共产生标准状况下气体2.24L,即0.1molNO2和NO气体,根据氮原子守恒,则反应过程中被还原的HNO3的物质的量为0.1mol,反应后生成的Cu(NO)3中含有NO3-的物质的量为2×![]() ,故参加反应的HNO3的物质的量为0.1mol+0.4mol=0.5molmol.;②铜与硝酸反应,生成硝酸铜,溶液中氢离子消耗完之后,仍然有硝酸根离子剩余,此时加入少量20%的稀硫酸,溶液相当于稀硝酸溶液,所以会发生铜片与稀硝酸的反应,反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
,故参加反应的HNO3的物质的量为0.1mol+0.4mol=0.5molmol.;②铜与硝酸反应,生成硝酸铜,溶液中氢离子消耗完之后,仍然有硝酸根离子剩余,此时加入少量20%的稀硫酸,溶液相当于稀硝酸溶液,所以会发生铜片与稀硝酸的反应,反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。

【题目】A,B,C,D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
阳离子 | Na+、Al3+、Ba2+、NH4+ |
阴离子 | Cl﹣、OH﹣、CO32﹣、SO42﹣ |
分别取四种物质进行实验,实验结果如下
①B溶液分别与C,D混合,均有白色沉淀生成;
②将A溶液逐滴滴入C溶液中,有沉淀生成,继续滴加A溶液时,沉淀减少直至完全消失;
③A与D两种固体混合加热有气体生成,该气体能使湿润的红色石蕊试液变蓝;
④用石墨电极电解B溶液,在阳极上产生一种有刺激性气味的气体.
(1)A所含的阴离子的电子式是 , B所含的阳离子是 .
(2)C的化学式是 , D的化学式是 .
(3)写出②中沉淀溶解的离子方程式 .