题目内容
【题目】随着工农业发展,NH4Cl的需求显著降低,价格低迷和产品积压导致利用“侯氏制碱法”生产的碱厂出现亏损。新联合制碱法在此基础上将氯元素转化为更有应用价值的HCl。

(1)气体X是__________。
(2)已知25℃时部分物质的溶解度数据:
物质 | NaCl | NaHCO3 | NH4Cl | NH4HCO3 |
溶解度/g | 36.0 | 10.3 | 39.5 | 24.8 |
结合表中数据说明过程Ⅰ中的反应能发生的原因是______________。
(3)过程Ⅰ获得的NaHCO3会吸附微量NH4Cl,导致产品Na2CO3中混有NaCl。
①用化学方程式表示过程Ⅱ中NaCl生成的原因:_____________。
②检验Na2CO3中NaCl的实验操作是,取少量固体于试管中_____________。
(4)过程Ⅲ以MgO为催化剂,在不同温度下加热灼烧,将NH4Cl分解为NH3和HCl。
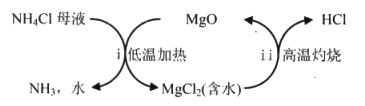
①步骤i中反应的化学方程式是____________。
②过程Ⅲ的优点是_____________。
【答案】CO2 25℃时,NaHCO3溶解度小,Na+与HCO3-结合生成NaHCO3更易从溶液中析出 NaHCO3+NH4Cl![]() NaCl+CO2↑+NH3↑+H2O 用水溶解,加入足量稀HNO3,再加入AgNO3溶液,如果产生白色沉淀则证明存在NaCl。 2NH4Cl+MgO
NaCl+CO2↑+NH3↑+H2O 用水溶解,加入足量稀HNO3,再加入AgNO3溶液,如果产生白色沉淀则证明存在NaCl。 2NH4Cl+MgO![]() 2NH3↑+H2O↑+MgCl2 将需求低的NH4Cl在不同温度下加热,分别得到更有价值的HCl和NH3,NH3可循环使用
2NH3↑+H2O↑+MgCl2 将需求低的NH4Cl在不同温度下加热,分别得到更有价值的HCl和NH3,NH3可循环使用
【解析】
(1)碳酸氢钠分解生成碳酸钠和二氧化碳气体;
(2)25℃时,NaHCO3溶解度小,易生成固体而析出;
(3)加热时碳酸氢钠、氯化铵可分别生成氯化钠、氨气、二氧化碳;检验Na2CO3中NaCl,可加入硝酸后在加入硝酸银溶液检验;
(4)由转化关系判断,氯化铵和氧化镁反应生成氨气、水和氯化镁;过程Ⅲ可得到氨气、氯化氢,氨气可循环使用。
(1)碳酸氢钠分解生成碳酸钠和二氧化碳气体,则X为二氧化碳;
(2)根据表中数据可知25℃时,NaHCO3溶解度小,Na+与HCO3-结合生成更难溶的NaHCO3固体,更易从溶液中析出;
(3)①加热时碳酸氢钠、氯化铵可分别生成氯化钠、氨气、二氧化碳,从而导致产品Na2CO3中混有NaCl,反应的化学方程式为NaHCO3+NH4Cl![]() NaCl+CO2↑+NH3↑+H2O;
NaCl+CO2↑+NH3↑+H2O;
②检验Na2CO3中的NaCl,可加入硝酸后在加入硝酸银溶液检验,操作方法是用水溶解,加入足量稀HNO3,再加入AgNO3溶液,如果产生白色沉淀则证明存在NaCl;
(4)①由转化关系判断,氯化铵和氧化镁反应生成氨气、水和氯化镁,反应的化学方程式为2NH4Cl+MgO![]() 2NH3↑+H2O↑+MgCl2;
2NH3↑+H2O↑+MgCl2;
②氯化铵需求较低,过程Ⅲ可得到更有价值的氨气、氯化氢,氨气可循环使用,即过程Ⅲ的优点是将需求低的NH4Cl在不同温度下加热,分别得到更有价值的HCl和NH3,NH3可循环使用。

【题目】(1)我国是世界上最早使用湿法炼铜的国家。湿法炼铜的原理是Fe+CuSO4=FeSO4+Cu,其中铁被__________(填“氧化”或“还原”),CuSO4作________(填“氧化”或“还原”)剂。在该反应中,若生成了1 mol Cu,消耗Fe的物质的量是_________。
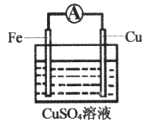
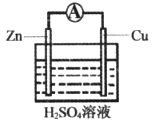
(2)某学习小组设计下图所示装置观察氧化还原反应中电子的转移。
实验Ⅰ | 实验Ⅱ | |
装置 |
|
|
现象 | 电流计指针向右偏转;铁片溶解; 铜片上有红色物质(铜)析出,铜片质量增加 | 电流计指针向右偏转;…… |
①实验Ⅰ中,Fe与CuSO4溶液反应的离子方程式是______________。
②根据实验Ⅰ的原理,推测实验Ⅱ中:锌片上发生_________(填“氧化”或“还原”)反应;铜片上的实验现象是__________。
【题目】电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示:
化学式 | HF | H2CO3 | H2S |
电离平衡常数 (Ka) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | K1=9.1×10-8 K2=1.1×10-12 |
(1)已知25℃时,①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH=-67.7kJ/mol,
②H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol,
氢氟酸电离的热化学方程式为________________________。
(2)将浓度为0.1 mol/L HF溶液加水稀释一倍(假设温度不变),下列各量增大的是____。
A.c(H+) B.c(H+)·c(OH-) C.![]() D.
D.![]()
(3)向Na2CO3溶液通入过量H2S,反应的离子方程式为______________。
(4)25℃时,在20mL 0.1mol/L氢氟酸中加入VmL 0.1mol/L NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是_____________。

A.pH=3的HF溶液和pH=11的NaF溶液中, 由水电离出的c(OH-)相等
B.①点时pH=6,此时溶液中, c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)< c(Na+)=0.1mol/L
(5)Na2CO3溶液显碱性是因为CO32-水解的缘故,请设计简单的实验证明之:_______________________。
(6)长期以来,一直认为氟的含氧酸不存在。1971年美国科学家用氟气通过细冰末时获得HFO,其结构式为H-O-F。HFO与水反应得到HF和化合物A,每生成1mol HF转移________mol电子。
(7)已知BiCl3水解产物中有 BiOCl生成。写出水解反应方程式___________________________,为防止其水解,如何配制 BiCl3溶液?_________________________________________________。