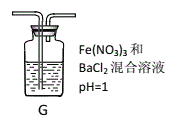
题目内容
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的( )
A.加入Al能放出H2的溶液中:ClO﹣、HCO ![]() 、SO
、SO ![]() 、NH
、NH ![]()
B.pH=2的溶液中:Fe2+、Na+、Mg2+、NO ![]()
C.能使KSCN溶液变红的溶液中:Na+、I﹣、NO ![]() 、HCO
、HCO ![]()
D.由水电离出的c(OH﹣)=1.0×10﹣13mol?L﹣1的溶液中:Na+、Ba2+、Cl﹣、Br﹣
【答案】D
【解析】解:A.加入Al能放出H2的溶液可能呈酸性或碱性,无论呈酸性还是碱性,HCO ![]() 都不能大量共存,故A错误; B.pH=2的溶液呈酸性,酸性条件下Fe2+、NO
都不能大量共存,故A错误; B.pH=2的溶液呈酸性,酸性条件下Fe2+、NO ![]() 发生氧化还原反应,故B错误;
发生氧化还原反应,故B错误;
C.能使KSCN溶液变红的溶液含有Fe3+ , 与I﹣发生氧化还原反应,与HCO ![]() 发生互促水解反应,故C错误;
发生互促水解反应,故C错误;
D.由水电离出的c(OH﹣)=1.0×10﹣13molL﹣1的溶液可能呈酸性或碱性,离子之间不发生任何反应,可大量共存,故D正确.
故选D.

 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案【题目】氮可形成多种气态氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是 ![]() 和
和 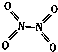 .实验测得N﹣N键的键能为167kJmol﹣1 , NO2中氮氧键的键能为 466kJmol﹣1 , N2O4中氮氧键的键能为438.5kJmol﹣1 .
.实验测得N﹣N键的键能为167kJmol﹣1 , NO2中氮氧键的键能为 466kJmol﹣1 , N2O4中氮氧键的键能为438.5kJmol﹣1 .
(1)写出N2O4转化NO2为的热化学方程式 .
(2)对反应N2O4(g)2NO2(g),在温度T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.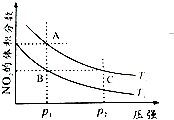
①A、C两点的反应速率v(A)v(C)(填“>”“=”或“<”).
②B、C两点的气体平均相对分子质量M(B)M(C)(填“>”、“=”或“<”).
③由状态B到达状态A可用的方法是 .
④A点气体的颜色比C点(填“深”、“浅”或“相同”),原因是 .
(3)在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到下表所示数据.
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
①在上述条件下,从反应开始直至20s时,v(NO2)=molL﹣1s﹣1 .
②若在相同的情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度应是molL﹣1 .