题目内容
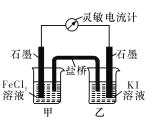
【题目】CO2通入BaCl2溶液中并不产生沉淀,在下图右侧的Y形管中放置合适的药品,进行合理操作,在BaCl2溶液中可以看到白色沉淀.右侧Y形管中放的药品是( )

A. Cu和浓硝酸 B. CaO和浓氮水
C. Na2SO3和较浓硫酸 D. KMnO4溶液和浓盐酸
【答案】B
【解析】
A. Cu和浓硝酸反应生成NO2,通入水中生成硝酸,硝酸和氯化钡以及二氧化碳均不反应,故A错误;
B. CaO和浓氮水反应会生成氨气,氨气通入溶液和二氧化碳反应生成碳酸铵,碳酸铵和氯化钡反应生成碳酸钡沉淀,故B正确;
C. Na2SO3和较浓硫酸反应生成二氧化硫,二氧化硫和氯化钡以及二氧化碳均不反应,故C错误;
D. KMnO4溶液和浓盐酸反应生成氯气,氯气和氯化钡以及二氧化碳均不反应,故D错误。
故选B。

练习册系列答案
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
【题目】根据下列实验操作和实验现象所得到的实验结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向亚硫酸钠试样中滴入盐酸酸化的Ba(C1O)2溶液 | 产生白色沉淀 | 试样已氧化变质 |
B | 向氯仿样品中加入硝酸银溶液 | 有白色沉淀产生 | 样品已变质 |
C | 向待测液中依次滴入氯水和KSCN溶液 | 溶液变为红色 | 待测液中含有Fe2+ |
D | 向NaHCO3溶液中滴加NaAlO2溶液 | 有白色沉淀和气体产生 | AlO2-与HCO3-发生了双水解反应 |
A. AB. BC. CD. D