题目内容
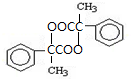
17.将 转变为
转变为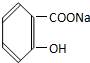 ,下列操作正确的是( )
,下列操作正确的是( )| A. | 与氢氧化钠共热后通足量的二氧化碳 | |
| B. | 溶解,加热通足量的二氧化硫气体 | |
| C. | 与稀硫酸共热后加足量氢氧化钠 | |
| D. | 与稀硫酸共热后加足量碳酸钠 |
分析 将 转变为
转变为 ,酯基转化为酚羟基,酯基水解需要在NaOH溶液中进行,酯基转化为-ONa,再利用二氧化碳和酚钠反应生成-OH即可,据此分析解答.
,酯基转化为酚羟基,酯基水解需要在NaOH溶液中进行,酯基转化为-ONa,再利用二氧化碳和酚钠反应生成-OH即可,据此分析解答.
解答 解:A. 与NaOH溶液共热后,酯基转化为-ONa,酚的酸性大于碳酸氢根离子而小于碳酸,所以-ONa和碳酸反应生成-OH,然后向共热后的溶液中通足量的二氧化碳即可实现,故A正确;
与NaOH溶液共热后,酯基转化为-ONa,酚的酸性大于碳酸氢根离子而小于碳酸,所以-ONa和碳酸反应生成-OH,然后向共热后的溶液中通足量的二氧化碳即可实现,故A正确;
B.溶解通入足量二氧化硫时,二氧化硫和水反应生成亚硫酸促进酯基水解,且亚硫酸酸性大于苯甲酸,所以-COONa和酯基分别转化为-COOH、-OH,故B错误;
C.与稀硫酸共热后,-COONa、酯基都转化为-COOH、-OH,然后加足量氢氧化钠,又转化为-COONa、-ONa,故C错误;
D.与稀硫酸共热后,-COONa、酯基都转化为-COOH、-OH,加足量碳酸钠,又转化为-COONa、-ONa,故D错误;
故选A.
点评 本题考查有机物的结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,注意酚羟基能和碳酸钠反应生成-ONa,但和碳酸氢钠不反应,为易错点.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
8.下列物质与常用危险化学品的类别不对应的是( )
| A. | CH4、C2H4--易燃液体 | B. | H2SO4、NaOH--腐蚀品 | ||
| C. | CaC2、Na--遇湿易燃物品 | D. | KMnO4、K2Cr2O7--氧化剂 |
5.Na2O2、CaC2、CaH2、FeS2均为离子化合物,前三种物质极易与水反应下列有关叙述中正确的是( )
| A. | 1molNa2O2与水反应转移2mol电子 | |
| B. | CaH2在水中以Ca2+和H-离子形式存在 | |
| C. | 四种化合物晶体类型和化学键类型均相同 | |
| D. | FeS2阴离子电子式为 |
12.下列各装置中铜电极上能产生气泡的是( )
| A. | 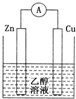 | B. | 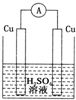 | ||
| C. | 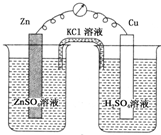 | D. |  |
2.可逆反应A(g)+3B(g)?2C(g)(正反应为放热反应)处于平衡状态,下列条件中可以提高A 的转化率的是:①高温②低温③高压④低压⑤加催化剂⑥除去C⑦增加A ⑧增加B( )
| A. | ①③⑤⑦ | B. | ②④⑥⑧ | C. | ②③⑥⑧ | D. | ②④⑤⑦ |
6.下列有关“电离平衡”的叙述中正确的是( )
| A. | 电解质在溶液里达到电离平衡时,溶质电离出的离子浓度相等 | |
| B. | 电离平衡时,由于分子和离子的浓度不断发生变化,所以说电离平衡是动态平衡 | |
| C. | 电离平衡时,弱电解质分子电离成离子的速率为零 | |
| D. | 电解质达到电离平衡后,各种离子的浓度不再变化 |
7.下列说法不正确的是( )
| A. | HCl、HBr、HI的熔、沸点依次升高与分子间作用力大小有关 | |
| B. | H2O的熔、沸点高于H2S是由于H2O分子之间存在氢键 | |
| C. | 甲烷可与水形成氢键 | |
| D. | I2易溶于CCl4可以用相似相溶原理解释 |
 苹果酸是一种常见的有机酸,其结构简式如图
苹果酸是一种常见的有机酸,其结构简式如图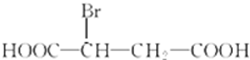 +H2O$\stackrel{一定条件}{→}$
+H2O$\stackrel{一定条件}{→}$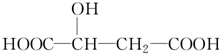 +HBr.
+HBr.
 出发合成A,其合成路线如下:已知:A在酸性条件下水解生成有机物B和甲醇.
出发合成A,其合成路线如下:已知:A在酸性条件下水解生成有机物B和甲醇.
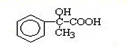 .
.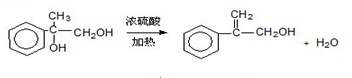 .
. .
.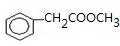 .
.