题目内容
【题目】葡萄酒中SO2最大使用量为0.25 g·L-1,取300.00 mL葡萄酒,通过适当的方法使所含SO2全部逸出并用H2O2将其全部氧化为H2SO4,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定。
(1)滴定前排气泡时,应选择下图中的________(填序号)。
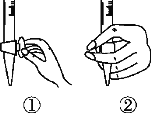
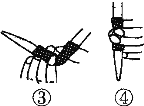
(2)若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积______(填序号)。
①=10 mL ②=40 mL ③<10 mL ④>40 mL。
(3)上述滴定实验中,可选择_______为指示剂,选择该指示剂时如何判断反应到达滴定终点:______
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为________g·L-1。滴定终点读数时俯视刻度线,则测量结果比实际值________(填“偏高”、“偏低”或“无影响”)。
【答案】③ ④ 酚酞 当加入最后一滴标准溶液后,溶液恰好变红色,且在半分钟内无变化,说明到达滴定终点 0.24 偏低
【解析】
(1)氢氧化钠是强碱,应用碱式滴定管量取;
(2)滴定管0刻度在上,且下端有一段没有刻度线;
(3)强碱滴定酸用酚酞;
(4)由SO2~H2SO4~2NaOH关系计算。滴定管0刻度在上,俯视读数偏小,标准液体积偏小。
(1)氢氧化钠是强碱,应用碱式滴定管量取,排液时应将橡皮管向上弯曲排出气泡,答案选③;
(2)滴定管0刻度在上,且下端有一段没有刻度线,故管内液体的体积大于40 mL,答案选④;
(3)强碱滴定酸用酚酞,滴定至终点时溶液的pH在酚酞的变色范围内,故可选用酚酞作指示剂。选择酚酞时反应到达滴定终点现象为:当加入最后一滴标准溶液后,溶液恰好变红色,且在半分钟内无变化;
(4)SO2与NaOH存在如下关系:
SO2 ~ H2SO4 ~ 2NaOH
64 g 2 mol
m(SO2) 0.090 0 mol·L-1×0.025 L
解得:m(SO2)=![]() =0.072 g,故葡萄酒中SO2的含量为
=0.072 g,故葡萄酒中SO2的含量为![]() ==0.24 g·L-1。滴定管0刻度在上,俯视读数偏小,标准液体积偏小,故测量结果比实际值偏低。
==0.24 g·L-1。滴定管0刻度在上,俯视读数偏小,标准液体积偏小,故测量结果比实际值偏低。

【题目】下表是元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题。
族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)②的原子结构示意图是___________。
(2)化学性质最不活泼的元素是___________(填元素符号)。
(3)③和④原子中,原子半径较大的是___________(填元素符号)。
(4)常用作半导体材料的是___________(填名称)。
(5)⑧、⑨的最高价氧化物对应的水化物中酸性较强的是_________(填化学式)。
(6)焰色反应显黄色的物质所含的金属元素是___________(填元素符号)。
(7)元素最高价氧化物对应的水化物中,呈两性的是___________(填化学式)。
(8)结构简式为![]() 的有机物分子式是_____,其中碳元素与氢元素的质量比m(C)∶(H)=________。
的有机物分子式是_____,其中碳元素与氢元素的质量比m(C)∶(H)=________。
【题目】丙酮的碘代反应![]() 的速率方程为
的速率方程为![]() ,其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为
,其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为![]() 改变反应物浓度时,反应的瞬时速率如表所示。
改变反应物浓度时,反应的瞬时速率如表所示。
|
|
|
0.25 | 0.050 | 1.4 |
0.50 | 0.050 | 2.8 |
1.00 | 0.050 | 5.6 |
0.50 | 0.100 | 2.8 |
下列说法正确的是( )
A.速率方程中的![]() 、
、![]()
B.该反应的速率常数![]()
C.增大![]() 的浓度,反应的瞬时速率加快
的浓度,反应的瞬时速率加快
D.在过量的![]() 存在时,反应掉87.5%的
存在时,反应掉87.5%的![]() 所需的时间是375min
所需的时间是375min