题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 10g质量分数为46%的乙醇溶液中,氢原子的总数约为0.6NA
B. 7.8gNa2O2与足量的水(H218O)反应生成的氧气所含的中子数为0.5NA
C. 将1L 0.1mol·L1 FeCl3溶液滴入沸水中,制得的Fe(OH)3胶粒数目为0.1NA
D. 常温下,NH![]() 数目:1L 0.5mol·L1 NH4Cl溶液大于2L 0.25mol·L1 NH4Cl溶液
数目:1L 0.5mol·L1 NH4Cl溶液大于2L 0.25mol·L1 NH4Cl溶液
【答案】D
【解析】
A.乙醇溶液中除了乙醇溶质中含有氢原子外,溶剂水也含有氢原子,因此10g质量分数为46%的乙醇溶液中,氢原子的总数大于0.6NA,故A错误;
B.Na2O2与足量的水(H218O)反应中,水既不做氧化剂也不做还原剂,因此氧气的来源是Na2O2中-1价的氧,因此7.8gNa2O2物质的量为0.1mol,生成氧气0.05 mol,所含的中子数为0.05×2×(16-8)×NA=0.8NA,故B错误;
C.Fe(OH)3胶粒是许多Fe(OH)3分子的集合体,所以将1L0.1mol/LFeCl3溶液滴入沸水中,制得的Fe(OH)3胶粒数目小于0.1NA,故C错误;
D.稀释有利于盐类水解,常温下,1L0.5mol/LNH4Cl溶液与2L0.25mol/LNH4Cl溶液中的NH4+的水解程度,前者小于后者,所以NH4+数目前者大于后者,故D正确。
综上所述,本题选D。

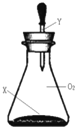
【题目】如图所示,常温时将一滴管液体Y一次性全部挤到充满O2的锥形瓶内(装置气密性良好),若锥形瓶内气体的最大物质的量是a mol,久置后其气体的物质的量是b mol,其中a≥b的是
X | Y |
| |
A | 少量C、Fe屑 | NaCl溶液 | |
B | 过量Na2SO3粉末 | 稀H2SO4 | |
C | 少量Fe块 | 浓H2SO4 | |
D | 过量Cu粉末 | 浓HNO3 |
A. A B. B C. C D. D