题目内容
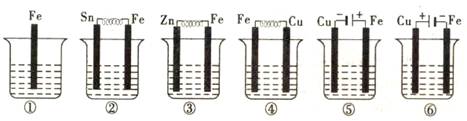
(Ⅰ)下列装置能组成原电池的是_____________ (填序号)

(Ⅱ)如上图④所示,若是原电池,请回答下列问题(若不是原电池,则不用回答)。
(1)负极材料是_______________________
(2)正极的电极反应式为________________________
(3)电池工作时总反应的离子方程式是____________________________
(4)导线中电子的流向________________________________
(5)阳离子的移动方向___________________________________
(6)该装置将 能转化为 能。

(Ⅱ)如上图④所示,若是原电池,请回答下列问题(若不是原电池,则不用回答)。
(1)负极材料是_______________________
(2)正极的电极反应式为________________________
(3)电池工作时总反应的离子方程式是____________________________
(4)导线中电子的流向________________________________
(5)阳离子的移动方向___________________________________
(6)该装置将 能转化为 能。
(12分) (Ⅰ)②④(2分)
(Ⅱ)(1) Cu (2分)
(2) Ag+ + e-=Ag (2分)
(3)Cu+2Ag+=2Ag+Cu2+ (2分)
(4)铜到银(或负极到正极)(1分)
(5)向正极(1分)(6)化学 电 (2分)
(Ⅱ)(1) Cu (2分)
(2) Ag+ + e-=Ag (2分)
(3)Cu+2Ag+=2Ag+Cu2+ (2分)
(4)铜到银(或负极到正极)(1分)
(5)向正极(1分)(6)化学 电 (2分)
试题分析:(Ⅰ)根据原电池的构成条件分析,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应。故能组成原电池的是②④。
(Ⅱ)(1)④中,Cu是负极,负极材料是Cu。
(2)Ag是正极,其电极式是Ag+ + e-=Ag。
(3)发生的反应是Cu置换Ag,离子方程式为Cu+2Ag+=2Ag+Cu2+。
(4)电子是由负极流向正极,即铜到银(或负极到正极)。
(5)阳离子向正极移动。
(6)装置能构成原电池,故该装置将化学能转化为电能。
点评:本题考查了原电池的构成条件及应用,这几个条件必须同时具备,缺一不可。

练习册系列答案
相关题目

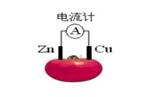
 Zn2+
Zn2+
 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是
电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是 。电池的总反应可表示为:
。电池的总反应可表示为:


