题目内容
请根据反应:Cu + 2FeCl3 = CuCl2 + 2FeCl2,设计一个原电池。
(1)画出装置图,标明两极材料和电解质溶液,并指出正、负极。
(2)写出两电极上的电极反应式。
(1)画出装置图,标明两极材料和电解质溶液,并指出正、负极。
(2)写出两电极上的电极反应式。
(1)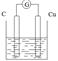 电解质溶液为FeCl3,C为正极,Cu为负极。
电解质溶液为FeCl3,C为正极,Cu为负极。
(2)负极(Cu):Cu - 2e- = Cu2+
正极(石墨):2Fe3+ + 2e- = 2Fe2+
 电解质溶液为FeCl3,C为正极,Cu为负极。
电解质溶液为FeCl3,C为正极,Cu为负极。(2)负极(Cu):Cu - 2e- = Cu2+
正极(石墨):2Fe3+ + 2e- = 2Fe2+
试题分析:(1)根据Cu + 2FeCl3 = CuCl2 + 2FeCl2,可知,Cu被氧化,2FeCl3被还原,所以设计的原电池为

电解质溶液为FeCl3,C为正极,Cu为负极;(2)电极上的反应为负极(Cu):Cu - 2e- = Cu2+
正极(石墨):2Fe3+ + 2e- = 2Fe2+
点评:本题考查了如果根据反应方程式设计原电池,是高考考查的重点,本题的起点高,落点低,相对比较容易。

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目



