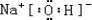��Ŀ����
11���л���A�ķ���ʽΪC9H10O2��A�ڹ�������������һ�����B��B���ӵĺ˴Ź�����������4��壬�������Ϊ2��2��2��3��B�ɷ�����ͼת����ϵ���������ԣ���
��֪����K���Ȼ�����Һ������ɫ��Ӧ���һ��ϵ�һԪȡ����ֻ�����ֽṹ��
�ڵ��ǻ���˫��̼ԭ������ʱ���ᷢ������ת����RCH=CHOH��RCH2CHO��
��ش��������⣺
��1��B�к��������ŵ���������������Ӧ�١���������ȡ����Ӧ���Ǣ٢ڣ�
��2��д���ṹ��ʽ��GCH3COOCH=CH2��ECH3COOH��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ����Ӧ�٣�
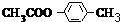 +Br2$\stackrel{����}{��}$
+Br2$\stackrel{����}{��}$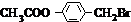 +HBr����Ӧ�ۣ�
+HBr����Ӧ�ۣ� ��
����4��ͬʱ��������Ҫ���K��ͬ���칹����3�֣�
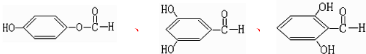
д����������һ��ͬ���칹��Ľṹ��ʽ��
 ����һ�ּ��ɣ�
����һ�ּ��ɣ������ϵ�һԪȡ����ֻ�����ֽṹ
���ܷ���������Ӧ
�����Ȼ�����Һ������ɫ��Ӧ��
���� G�ܷ���ˮ�ⷴӦ˵��G�к���������G�����Ӿ۷�Ӧ����������ϩ������G�Ľṹ��ʽΪ��CH3COOCH=CH2��G�Ȼ�����C��F��F�ܷ���������Ӧ����E��E������C����F��CH3CHO��C��CH3COONa��E��CH3COOH���л���A�ķ���ʽΪC9H10O2�������Ͷ�Ϊ$\frac{2��9+2-10}{2}$=5�����Ǻ��б�����A�ڹ������������ɵ�һ�ȴ���B��B����������ˮ��Һ����������������C��D��D����������������J��D���д��ǻ���A������������A�к���1��������1��������A�ڹ������������ɵ�һ�ȴ���B��A�������������K��һ±������ֻ������ͬ���칹�壬��AΪ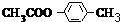 ��BΪ
��BΪ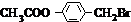 ��DΪ
��DΪ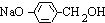 ��IΪ
��IΪ ��JΪ
��JΪ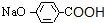 ��KΪ
��KΪ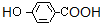 ��MΪ
��MΪ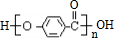 ���ݴ˽��
���ݴ˽��
��� �⣺G�ܷ���ˮ�ⷴӦ˵��G�к���������G�����Ӿ۷�Ӧ����������ϩ������G�Ľṹ��ʽΪ��CH3COOCH=CH2��G�Ȼ�����C��F��F�ܷ���������Ӧ����E��E������C����F��CH3CHO��C��CH3COONa��E��CH3COOH���л���A�ķ���ʽΪC9H10O2�������Ͷ�Ϊ$\frac{2��9+2-10}{2}$=5�����Ǻ��б�����A�ڹ������������ɵ�һ�ȴ���B��B����������ˮ��Һ����������������C��D��D����������������J��D���д��ǻ���A������������A�к���1��������1��������A�ڹ������������ɵ�һ�ȴ���B��A�������������K��һ±������ֻ������ͬ���칹�壬��AΪ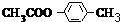 ��BΪ
��BΪ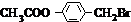 ��DΪ
��DΪ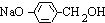 ��IΪ
��IΪ ��JΪ
��JΪ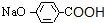 ��KΪ
��KΪ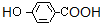 ��MΪ
��MΪ ��
��
��1��BΪ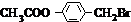 ����B�к�����������������������ΪA�ڹ������������ɵ�һ�ȴ���B��Ϊȡ����Ӧ����ΪB���������Ƶ�ˮ��Һ�з���ˮ�ⷴӦ��ҲΪȡ����Ӧ����Ϊ������Ӧ����Ϊ���۷�Ӧ����Ϊ�Ӿ۷�Ӧ����������ȡ����ӦΪ�٢ڣ�
����B�к�����������������������ΪA�ڹ������������ɵ�һ�ȴ���B��Ϊȡ����Ӧ����ΪB���������Ƶ�ˮ��Һ�з���ˮ�ⷴӦ��ҲΪȡ����Ӧ����Ϊ������Ӧ����Ϊ���۷�Ӧ����Ϊ�Ӿ۷�Ӧ����������ȡ����ӦΪ�٢ڣ�
�ʴ�Ϊ���������٢ڣ�
��2�������Ϸ�����GΪCH3COOCH=CH2��EΪCH3COOH��
�ʴ�Ϊ��CH3COOCH=CH2��CH3COOH��
��3����Ӧ�ٵķ���ʽΪ��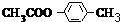 +Br2$\stackrel{����}{��}$
+Br2$\stackrel{����}{��}$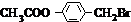 +HBr��
+HBr��
��Ӧ�۵ķ���ʽΪ��
�ʴ�Ϊ��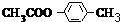 +Br2$\stackrel{����}{��}$
+Br2$\stackrel{����}{��}$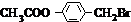 +HBr��
+HBr�� ��
��
��4��KΪ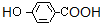 ��K��ͬ���칹����һ���ص㣬
��K��ͬ���칹����һ���ص㣬
�����ϵ�һԪȡ����ֻ�����ֽṹ��˵��������ֻ��һ�����͵���ԭ�ӣ�
���ܷ���������Ӧ˵������ȩ����
�����Ȼ�����Һ������ɫ��Ӧ˵�����з��ǻ���
�����������K��ͬ���칹���У� ��
��
���Թ���3��ͬ���칹�壬
�ʴ�Ϊ��3�� ����һ�ּ��ɣ�
����һ�ּ��ɣ�
���� �����л�����ƶϣ��Ƕ��л���֪ʶ���ۺ����ã���Ŀ����ij��Ӧ��ϢҪ��ѧ������Ӧ�ã��ܽϺõĿ��鿼�����Ķ�����ѧ������˼ά���������ȵ����ͣ��ѶȽϴ���G�ļӾ۲���Ľṹ��ʽ�ж�G�ķ���ʽ���ٸ���G�����ķ�Ӧ�����ʽ�ж�G�Ľṹ��ʽ���ƶϵĹؼ������������Ʒ������Ʒ�����ƶ��������ʣ�ע�������÷�Ӧ������

| A�� | X�ǵ�IAԪ�أ�Z�ǵڢ�AԪ�� | |
| B�� | Ԫ��X��Z�γɵĻ������ǹ��ۻ����� | |
| C�� | Yһ���ǽ���Ԫ�� | |
| D�� | Z������������Ӧ��ˮ���������� |
| A�� | ȼ�� | B�� | ȡ����Ӧ | C�� | �ӳɷ�Ӧ | D�� | ������Ӧ |
| A�� |  ���ڻ�״������ ���ڻ�״������ | B�� |  ����±���� ����±���� | ||
| C�� | 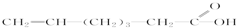 ������״������ ������״������ | D�� | 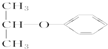 ������ ������ |
| A�� | ������������Ļ�������ڹ��������·�Ӧ�Ʊ������飨C2H5Cl�� | |
| B�� | ���Ҵ�Ѹ�ټ�����170���϶�����ϩ | |
| C�� | ����ԭ���ۡ�Һ��ͱ�������屽 | |
| D�� | �����ȴ����к��ȣ���NaOH��Һ���Ⱥ���ϡ�����ữ���ټ��� |
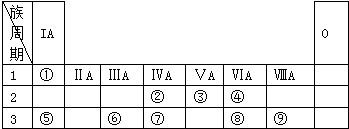
 ��W��ܵĵ����ڴ��������������·����ķ�Ӧ�ǹ�ҵ��ȡZ�Ļ�����д���÷�Ӧ�Ļ�ѧ����ʽ��4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
��W��ܵĵ����ڴ��������������·����ķ�Ӧ�ǹ�ҵ��ȡZ�Ļ�����д���÷�Ӧ�Ļ�ѧ����ʽ��4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
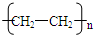 ����Ӧ����Ϊ�Ӿ۷�Ӧ��
����Ӧ����Ϊ�Ӿ۷�Ӧ��