题目内容
15.几种微粒具有相同的核电荷数,则可说明( )| A. | 核外电子数一定相等 | B. | 一定是同一元素 | ||
| C. | 彼此之间一定是同位素 | D. | 可能是同一元素 |
分析 几种微粒具有相同的核电荷数,可能为原子、离子、分子,若均为原子,互为同位素,可能为同一元素,若为电中性微粒,则核电荷数=核外电子数,若不是电中性微粒,则核电荷数不等于核外电子数,阳离子中核外电子数=质子数-电荷数,阴离子中核外电子数=质子数+电荷数.
解答 解:A.若为电中性微粒,核外电子数相等,若不是电中性微粒,则核外电子数不一定相等,如NH4+和Na,故A错误;
B.若均为原子,互为同位素,为同一元素,也可能不是原子,如H2O和HF,故B错误;
C.若均为原子,互为同位素,也可能不是原子,不一定是同位素,如OH-和F-,故C错误;
D.若均为原子,互为同位素,为同一元素,如12C和13C,故D正确,
故选:D.
点评 本题能考查核电荷数与核外电子数关系、元素与同位素概念等,有利于学生的发散思维能力培养,注意利用列举法进行解答,题目难度不大.

练习册系列答案
相关题目
6.将等质量的四块铜片在酒精灯上加热后,分别插入下列溶液中,放置片刻后铜片质量与加热前相同的是( )
| A. | 硝酸 | B. | 盐酸 | C. | 石灰水 | D. | 乙醇 |
3.目前下列工艺过程没有直接使用离子交换技术的是( )
| A. | 硬水的软化 | B. | 电解饱和食盐水制造NaOH | ||
| C. | 电渗析淡化海水 | D. | 海水中提取金属Mg |
7.同温同压下,xg的甲气体和Yg的乙气体占有相同的体积,根据阿伏伽德罗定律判断,下列叙述错误的是( )
| A. | x:y等于等质量的甲和乙的分子个数之比 | |
| B. | x:y等于同温同压下甲和乙的密度之比 | |
| C. | x:y等于甲与乙的相对分子质量之比 | |
| D. | x:y等于同温同体积下等质量的甲和乙的压强之比 |
4.下列说法错误的是( )
| A. | CCl4可由CH4制得,可萃取碘水中的碘 | |
| B. | 乙醇分子中含有醛基 | |
| C. | 75%的乙醇溶液常用于医疗消毒 | |
| D. | 只用水就能鉴别苯和四氯化碳 |
5.甲醇、天燃气是重要的化工原料,又可作为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇、甲烷.已知合成甲醇发生的主反应如下(已知CO的结构式为C≡O):
①CH3OH(g)?CO(g)+2H2(g)△H1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
③CO(g)+H2O(g)?CO2(g)+H2(g)△H3
回答下列问题:
(1)已知反应①中相关的化学键能数据如下:
由此计算△H1=+99kJ•mol-1.已知△H2=-58kJ•mol-1,则△H3=-41kJ•mol-1.
(2)在容积为1.00L的容器中,通入一定量的甲醇发生反应①.100℃时,体系中各物质浓度随时间变化如图1所示(平衡时甲醇的转化率记作a1).
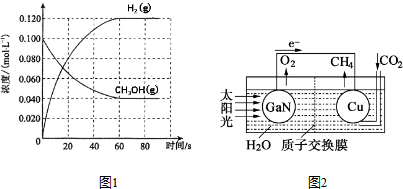
①在0-60s时段,反应速率v(CO)为0.001mol/(L•s)②;该反应的平衡常数K1 的计算式为$\frac{c(CO)c{\;}^{2}(H{\;}_{2})}{c(CH{\;}_{3}OH)}$.
②已知若在恒压条件下进行,平衡时CH3OH的转化率a2大于a1(填“大于”或“小于”、“等于”),判断理由是因为该反应为体积增大的反应,所以恒压相当于在恒容的基础上减小压强,平衡正向移动.
(3)合成CH4的原理:CO2(g)+4H2(g)?CH4(g)+2H2O(g)△H=-162kJ•mol-1.其他条件相同,实验测得在T1和P1与T2和P2条件下该反应的H2平衡转化率相同,若T1>T2,则P1>P2(填“>”、“<”或“=”).
(4)科学家用氮化镓材料与铜组装如图2所示的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4①写出铜电极表面的电极反应式CO2+8e-+8H+=CH4+2H2O;.
②为提高该人工光合系统的工作效率,可向装置中加入少量硫酸(选填“盐酸”或“硫酸”).
(5)标准状况下,将22.4L的甲烷完全燃烧生成的CO2通入到0.1L 1mol•L-1的NaOH溶液中,所得溶液中离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-).
①CH3OH(g)?CO(g)+2H2(g)△H1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
③CO(g)+H2O(g)?CO2(g)+H2(g)△H3
回答下列问题:
(1)已知反应①中相关的化学键能数据如下:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1076 | 465 | 413 |
(2)在容积为1.00L的容器中,通入一定量的甲醇发生反应①.100℃时,体系中各物质浓度随时间变化如图1所示(平衡时甲醇的转化率记作a1).

①在0-60s时段,反应速率v(CO)为0.001mol/(L•s)②;该反应的平衡常数K1 的计算式为$\frac{c(CO)c{\;}^{2}(H{\;}_{2})}{c(CH{\;}_{3}OH)}$.
②已知若在恒压条件下进行,平衡时CH3OH的转化率a2大于a1(填“大于”或“小于”、“等于”),判断理由是因为该反应为体积增大的反应,所以恒压相当于在恒容的基础上减小压强,平衡正向移动.
(3)合成CH4的原理:CO2(g)+4H2(g)?CH4(g)+2H2O(g)△H=-162kJ•mol-1.其他条件相同,实验测得在T1和P1与T2和P2条件下该反应的H2平衡转化率相同,若T1>T2,则P1>P2(填“>”、“<”或“=”).
(4)科学家用氮化镓材料与铜组装如图2所示的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4①写出铜电极表面的电极反应式CO2+8e-+8H+=CH4+2H2O;.
②为提高该人工光合系统的工作效率,可向装置中加入少量硫酸(选填“盐酸”或“硫酸”).
(5)标准状况下,将22.4L的甲烷完全燃烧生成的CO2通入到0.1L 1mol•L-1的NaOH溶液中,所得溶液中离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-).
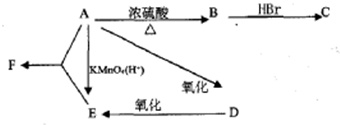 某有机物A,由C、H、O三种元素组成,在一定条件下由A可以转变为有机物B、C、D、E.转变关系如图所示.已知B是石油化工发展水平的标志.
某有机物A,由C、H、O三种元素组成,在一定条件下由A可以转变为有机物B、C、D、E.转变关系如图所示.已知B是石油化工发展水平的标志.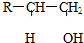 $→_{△}^{浓硫酸}$R-CH═CH2+H2O)
$→_{△}^{浓硫酸}$R-CH═CH2+H2O)