题目内容
19.用高锰酸钾标准溶液滴定加入稀硫酸酸化后的过氧化氢溶液,能测定溶液中过氧化氢的含量,并探究过氧化氢的性质.滴定过程中反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里.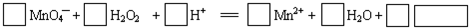
分析 由给出方程式可知,反应物中高锰酸钾有强氧化性,能将双氧水氧化为氧气,所以方程式中缺少的物质是O2,锰元素化合价由+7价降到+2价,降低了5价,双氧水中的氧元素从-1价升高到0价,依据氧化还原反应得失电子守恒规律及原子个数守恒规律配平方程式,据此解答.
解答 解:高锰酸钾有强氧化性,能将双氧水氧化为氧气,所以方程式中缺少的物质是O2,锰元素化合价由+7价降到+2价,降低了5价,双氧水中的氧元素从-1价升高到0价,生成1mol氧气时,氧元素化合价升高2价,根据氧化还原反应得失电子守恒规律,配平化学方程式高锰酸根前面的系数为2,双氧水前面的系数为5,根据原子守恒来配平其他物质前面的系数,该反应的化学方程式为:2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2,
故答案为:2;5;6;2;8;502.
点评 本题考查了氧化还原方程式的书写,明确氧化还原反应中得失电子守恒规律及原子个数守恒规律是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.高温条件下反应达到平衡时的平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.恒容条件下升高温度,H2浓度减小.则下列说法正确的是( )
| A. | 反应的热化学方程式可表示为:CO(g)+H2O(g)$?_{高温高压}^{催化剂}$CO2(g)+H2(g)△H<0 kJ/mol | |
| B. | 恒温恒容下,增大压强,H2浓度一定减小 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 该反应的正反应为放热反应 |
10.对化学反应3X(g)+Y(g)?2Z(g)+2Q(s)达到平衡后,增大压强,下列关于对该化学反应产生的影响的说法正确的是( )
| A. | 正反应速率增大,逆反应速率减小,平衡向正反应方向移动 | |
| B. | 正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 | |
| C. | 正、逆反应速率都增大,平衡向正反应方向移动 | |
| D. | 正、逆反应速率都没有变化,平衡不发生移动 |
7.在水溶液中能够大量共存的离子组是( )
| A. | Na+,Ca2+,HCO3-,OH- | B. | K+,NH4+,S2-,OH- | ||
| C. | Mg2+,K+,HSO3-,H+ | D. | K+,Na+,NO3-,CO32- |
4.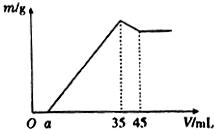 准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol•L-l的NaoH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示,则所用硫酸溶液的物质的量浓度为( )
准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol•L-l的NaoH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示,则所用硫酸溶液的物质的量浓度为( )
 准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol•L-l的NaoH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示,则所用硫酸溶液的物质的量浓度为( )
准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol•L-l的NaoH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示,则所用硫酸溶液的物质的量浓度为( )| A. | 3.50mol/L | B. | 1.75mol/L | C. | 0.85mol/L | D. | 无法计算 |
11.下列各组微粒中,核外电子总数相等的是( )
| A. | O3和CO2 | B. | OH-和Al3+ | C. | NO和CO | D. | Cl-和Ne |
6.下列事实可证明氨水是弱碱的是( )
| A. | 氨水能跟氯化亚铁溶液反应生成氢氧化亚铁 | |
| B. | 铵盐受热易分解 | |
| C. | 0.1 mol/L氨水可以使酚酞试液变红 | |
| D. | 常温下,0.1 mol/L氨水的pH约为9 |