题目内容
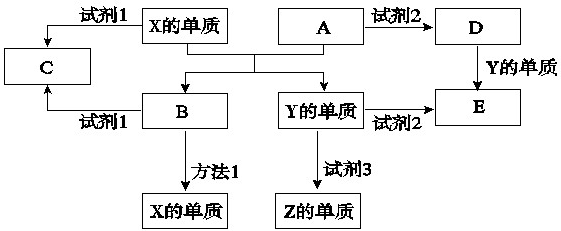
A、B、C、D、E是中学常见的5种化合物,A、B是金属氧化物且A是红棕色固体,元素X、Y、Z是中学化学中常见的单质,相关物质间的关系如图所示.
(1)工业上得到单质X的冶炼方法1是
(2)单质X与试剂1、单质Y与试剂2都能产生Z单质,试剂3是生活中常见的液体,请写出Y与试剂3反应的化学方程式是
(3)若试剂1是NaOH溶液,单质X与试剂1反应的离子方程式
(4)若试剂2是盐酸.
①如何检验D物质中的金属阳离子
②将D的饱和溶液滴加到沸水中得到有丁达尔效应的分散系,用离子方程式和平衡移动理论说明产生这种分散系的原因

(1)工业上得到单质X的冶炼方法1是
电解
电解
.(2)单质X与试剂1、单质Y与试剂2都能产生Z单质,试剂3是生活中常见的液体,请写出Y与试剂3反应的化学方程式是
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
.
| ||
(3)若试剂1是NaOH溶液,单质X与试剂1反应的离子方程式
2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
.(4)若试剂2是盐酸.
①如何检验D物质中的金属阳离子
取少量D溶液于试管中,再向试管中滴加少量的硫氰化钾溶液,若溶液显红色,则D物质中的金属阳离子是Fe3+
取少量D溶液于试管中,再向试管中滴加少量的硫氰化钾溶液,若溶液显红色,则D物质中的金属阳离子是Fe3+
.②将D的饱和溶液滴加到沸水中得到有丁达尔效应的分散系,用离子方程式和平衡移动理论说明产生这种分散系的原因
D溶液存在Fe3++3H2O?Fe(OH)3+3H+水解平衡,且正反应是吸热反应,当其滴加到沸水中时使平衡向正向移动,产生大量的Fe(OH)3凝结成胶体颗粒,而有丁达尔效应
D溶液存在Fe3++3H2O?Fe(OH)3+3H+水解平衡,且正反应是吸热反应,当其滴加到沸水中时使平衡向正向移动,产生大量的Fe(OH)3凝结成胶体颗粒,而有丁达尔效应
.分析:A是金属氧化物且A是红棕色固体,则A是氧化铁,A和X发生置换反应生成B,B是金属氧化物,则该反应是铝和氧化铁发生铝热反应,则X是铝,Y是铁,B是氧化铝,铝和氧化铝都与试剂1反应生成C,用电解氧化铝的方法冶炼铝;
Al、氧化铝都既能与酸反应又能与碱反应,而Fe、氧化铁都能与酸反应,则试剂1为NaOH溶液时,C为偏铝酸钠;试剂2为盐酸时,D为氯化铁、E为氯化亚铁,最后结合化学用语来解答即可.
Al、氧化铝都既能与酸反应又能与碱反应,而Fe、氧化铁都能与酸反应,则试剂1为NaOH溶液时,C为偏铝酸钠;试剂2为盐酸时,D为氯化铁、E为氯化亚铁,最后结合化学用语来解答即可.
解答:解:A是金属氧化物且A是红棕色固体,则A是氧化铁,A和X发生置换反应生成B,B是金属氧化物,则该反应是铝和氧化铁发生铝热反应,则X是铝,Y是铁,B是氧化铝,铝和氧化铝都与试剂1反应生成C,用电解氧化铝的方法冶炼铝;
Al、氧化铝都既能与酸反应又能与碱反应,而Fe、氧化铁都能与酸反应,则试剂1为NaOH溶液时,C为偏铝酸钠;试剂2为盐酸时,D为氯化铁、E为氯化亚铁;
(1)工业采用电解熔融氧化铝的方法冶炼铝,故答案为:电解;
(2)单质X与试剂1、单质Y与试剂2都能产生Z单质,则Z是氢气,试剂3是生活中常见的液体,则为水,高温下,铁和水蒸气反应生成四氧化三铁和氢气,反应方程式为:3Fe+4H2O(g)
Fe3O4+4H2,
故答案为:3Fe+4H2O(g)
Fe3O4+4H2;
(3)若试剂1是NaOH溶液,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,离子反应方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)若试剂2是盐酸,
①氧化铁和盐酸反应生成氯化铁,铁离子和硫氰化钾溶液反应生成血红色溶液,检验方法为:取少量D溶液于试管中,再向试管中滴加少量的硫氰化钾溶液,若溶液显红色,则D物质中的金属阳离子是Fe3+,
故答案为:取少量D溶液于试管中,再向试管中滴加少量的硫氰化钾溶液,若溶液显红色,则D物质中的金属阳离子是Fe3+;
②氯化铁是强酸弱碱盐,易水解生成氢氧化铁,且盐类的水解反应是吸热反应,升高温度促进盐类水解,从而产生大量的Fe(OH)3凝结成胶体颗粒,而有丁达尔效应,
故答案为:D溶液存在Fe3++3H2O?Fe(OH)3+3H+水解平衡,且正反应是吸热反应,当其滴加到沸水中时使平衡向正向移动,产生大量的Fe(OH)3凝结成胶体颗粒,而有丁达尔效应.
Al、氧化铝都既能与酸反应又能与碱反应,而Fe、氧化铁都能与酸反应,则试剂1为NaOH溶液时,C为偏铝酸钠;试剂2为盐酸时,D为氯化铁、E为氯化亚铁;
(1)工业采用电解熔融氧化铝的方法冶炼铝,故答案为:电解;
(2)单质X与试剂1、单质Y与试剂2都能产生Z单质,则Z是氢气,试剂3是生活中常见的液体,则为水,高温下,铁和水蒸气反应生成四氧化三铁和氢气,反应方程式为:3Fe+4H2O(g)
| ||
故答案为:3Fe+4H2O(g)
| ||
(3)若试剂1是NaOH溶液,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,离子反应方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)若试剂2是盐酸,
①氧化铁和盐酸反应生成氯化铁,铁离子和硫氰化钾溶液反应生成血红色溶液,检验方法为:取少量D溶液于试管中,再向试管中滴加少量的硫氰化钾溶液,若溶液显红色,则D物质中的金属阳离子是Fe3+,
故答案为:取少量D溶液于试管中,再向试管中滴加少量的硫氰化钾溶液,若溶液显红色,则D物质中的金属阳离子是Fe3+;
②氯化铁是强酸弱碱盐,易水解生成氢氧化铁,且盐类的水解反应是吸热反应,升高温度促进盐类水解,从而产生大量的Fe(OH)3凝结成胶体颗粒,而有丁达尔效应,
故答案为:D溶液存在Fe3++3H2O?Fe(OH)3+3H+水解平衡,且正反应是吸热反应,当其滴加到沸水中时使平衡向正向移动,产生大量的Fe(OH)3凝结成胶体颗粒,而有丁达尔效应.
点评:本题考查无机物的推断,明确铝热反应及Al、氧化铝、Fe、氧化铁的性质即可解答,并注意试剂1可以为酸或强碱来分析解答,题目难度不大.

练习册系列答案
相关题目
已知A、B、C、D、E是短周期原子序数依次增大的五种元素,A原子在元素周期表中原子半径最小,B与E同主族,且E的原子序数是B的两倍,C、D是金属,它们的氢氧化物均难溶于水.下列说法不正确的是( )
| A、简单离子的半径:C>D>E>B | B、工业上常用电解法制得C和D的单质 | C、稳定性:A2B>A2E | D、单质D可用于冶炼某些难熔金属 |

 2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热
2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热
