题目内容
11.下列离子方程式错误的是( )| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| B. | 等物质的量的MgCl2、Ba(OH)2 和 HC1溶液混合:Mg2++2OH-=Mg(OH)2↓ | |
| C. | 酸性介质中KMnO4氧化 H2O2:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O | |
| D. | 二氧化硫通入次氯酸钠溶液:SO2+ClO-+2OH-=SO42-+Cl-+H2O |
分析 A.二者反应生成硫酸钡和水;
B.先发生中和反应,氢氧根离子有一半没有发生中和反应,剩余的氢氧根离子和镁离子反应生成氢氧化镁沉淀;
B.二者发生氧化还原反应生成锰离子、氧气和水;
D.二者发生氧化还原反应生成硫酸根离子和氯离子.
解答 解:A.二者反应生成硫酸钡和水,离子方程式为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故A正确;
B.先发生中和反应,氢氧根离子有一半没有发生中和反应,剩余的氢氧根离子和镁离子反应生成氢氧化镁沉淀,离子方程式为Mg2++2H++4OH-=Mg(OH)2↓+2H2O,故B错误;
B.二者发生氧化还原反应生成锰离子、氧气和水,离子方程式为2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O,故C正确;
D.二者发生氧化还原反应生成硫酸根离子和氯离子,离子方程式为SO2+ClO-+2OH-=SO42-+Cl-+H2O,故D正确;
故选B.
点评 本题考查离子方程式正误判断,为高频考点,侧重考查学生分析判断及应用能力,明确离子方程式书写特点及物质性质是解本题关键,易错选项是BD,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.苯甲酸甲酯是一种重要的工业原料,有机化学中通过酯化反应原理,可以进行苯甲酸甲酯的合成.有关物质的物理性质、实验装置如下所示:

实验一:制取苯甲酸甲酯:在大试管中加入15g苯甲酸和一定量的甲醇,边振荡边缓慢加入一定量浓硫酸,按图A连接仪器并实验.
(1)苯甲酸与甲醇反应的化学方程式为 .
.
(2)大试管Ⅰ中除了装有15g苯甲酸和一定量的甲醇和沸石外还需要加入一定量浓硫酸,浓硫酸的作用是催化剂和吸水剂.
(3)实验室制取乙酸乙酯时,为了除去乙酸乙酯中混有的乙酸所用试剂为饱和碳酸钠溶液.
实验二:提纯苯甲酸甲酯:该实验要先把图A中制备的苯甲酸甲酯水洗提纯,再利用图B装置进行蒸馏提纯
(4)水洗提纯时所进行的操作为(填操作名称)分液.
(5)用图B装置进行蒸馏提纯时,当温度计显示199.6时,可用锥形瓶收集苯甲酸甲酯.
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |

实验一:制取苯甲酸甲酯:在大试管中加入15g苯甲酸和一定量的甲醇,边振荡边缓慢加入一定量浓硫酸,按图A连接仪器并实验.
(1)苯甲酸与甲醇反应的化学方程式为
 .
.(2)大试管Ⅰ中除了装有15g苯甲酸和一定量的甲醇和沸石外还需要加入一定量浓硫酸,浓硫酸的作用是催化剂和吸水剂.
(3)实验室制取乙酸乙酯时,为了除去乙酸乙酯中混有的乙酸所用试剂为饱和碳酸钠溶液.
实验二:提纯苯甲酸甲酯:该实验要先把图A中制备的苯甲酸甲酯水洗提纯,再利用图B装置进行蒸馏提纯
(4)水洗提纯时所进行的操作为(填操作名称)分液.
(5)用图B装置进行蒸馏提纯时,当温度计显示199.6时,可用锥形瓶收集苯甲酸甲酯.
2.在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液生成沉淀的量与滴入NaOH溶液的体积关系如图所示则原混合溶液中Al2(S04)3与MgSO4中SO42-的物质的量浓度之比为( )

| A. | 6:1 | B. | 3:1 | C. | 3:4 | D. | 3:2 |
19.如图,有机化合物Ⅰ转化为Ⅱ的反应类型是( )


| A. | 氧化反应 | B. | 还原反应 | C. | 取代反应 | D. | 水解反应 |
6.有机物M是苯的同系物,其结构为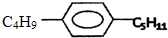 ,则M可能的结构简式共有( )
,则M可能的结构简式共有( )
 ,则M可能的结构简式共有( )
,则M可能的结构简式共有( )| A. | 6种 | B. | 12种 | C. | 24种 | D. | 32种 |
16.对于反应2SO2(g)+O2(g)?2SO3(g)能增大正反应速率的措施是( )
| A. | 移去部分SO3 | B. | 增大容器容积 | C. | 降低体系温度 | D. | 通入大量O2 |
3.物质的量浓度都是0.1mol/L的下列溶液,酸性最强的是( )
| A. | HCl | B. | H2SO4 | C. | CH3COOH | D. | ( NH4)2SO4 |
20.下列说法不正确的是( )
| A. | 为除去FeSO4溶液中的Fe2(SO4)3,可加入铁粉,再过滤 | |
| B. | SO2使溴水褪色,不能说明SO2具有漂白性 | |
| C. | HCl、NO2溶于水都有化学键断裂,但不全属于化学变化 | |
| D. | 为除去CO2中少量的SO2,可使其通过饱和Na2CO3溶液 |
1.下列变化过程,属于放热过程的是( )
| A. | 合成氨反应 | B. | 液态水变成水蒸气 | ||
| C. | 弱酸弱碱的电离 | D. | 灼热的炭与CO2的反应 |