题目内容
【题目】设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A.l mol硫酸钾中阴离子所带电荷数为NA
B.乙烯(C2H4)和环丙烷(C3H6)组成的28g混合气体中含有4NA个氢原子
C.22.4L氯气和足量氢气反应转移的电子数为2NA
D.将0.1mol氯化铁溶于1L水中,所得溶液含有0.2NA个Cl-
【答案】B
【解析】
A、1mol硫酸钾中含有阴离子硫酸根离子的物质的量为1mol,1mol硫酸根离子带有2mol负电荷,所带电荷数为2NA,故A错误;
B、乙烯(C2H4)和环丙烷(C3H6)的实验式均为CH2,28g混合气体中含有CH2原子团的物质的量为![]() =2mol,含有4mol氢原子,所以28 g混合气体中含有4NA个氢原子,故B正确;
=2mol,含有4mol氢原子,所以28 g混合气体中含有4NA个氢原子,故B正确;
C、未告知温度和压强,气体摩尔体积不一定为22.4L/mol,无法计算22.4L氯气的物质的量,因此无法计算转移的电子数,故C错误;
D、氯化铁的化学式为FeCl3,将0.1mol氯化铁溶于1L水中完全电离,所得溶液含有Cl-0.3NA,故D错误;
故选B。

【题目】下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480 mL0.2 molL-1的稀硫酸。可供选用的仪器有:①托盘天平;②烧瓶;③烧杯;④药匙;⑤量筒;⑥玻璃棒。

(1)配制稀硫酸时,还缺少的仪器有________________(写仪器名称),
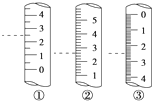
(2)下图是某些仪器的刻度部分示意图,其中为量筒的是________(填编号)。配制稀硫酸需要用量筒量取上述浓硫酸的体积为________mL,量取硫酸时应选用________(填选项)规格的量筒。
A.10mL B.50mL C.100mL D.200mL
(3)下图为量取浓硫酸后配制稀硫酸的操作示意图,其正确的操作步骤为_______(填编号)。
|
|
|
|
|
|
① | ② | ③ | ④ | ⑤ | ⑥ |
(4)对所配制的稀硫酸进行测定,发现其浓度大于0.2 mol/L,引起该误差的原因可能是_____。
A.所用的浓硫酸长时间放置在密封不好的容器中
B.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
C.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
D.将稀释后的稀硫酸未冷却立即转入容量瓶后,紧接着就进行以后的实验操作
E.定容时,俯视容量瓶刻度线进行定容