��Ŀ����
 ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺��1����X��Y���Ƕ��Ե缫��a��100mL����NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
�ٵ�����X���ϵĵ缫��ӦʽΪ
2H++2e-=H2��
2H++2e-=H2��
����Y�缫�ϵĵ缫��ӦʽΪ
2Cl--2e-=Cl2��
2Cl--2e-=Cl2��
����һ��ʱ����������õ�112mL��״���µ����壬��ʱ��Һ��pHΪ
13
13
������Һ����仯���Բ��ƣ�
��2����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��X�缫�IJ�����
��ͭ
��ͭ
���缫��Ӧʽ��Cu2++2e-=Cu
Cu2++2e-=Cu
����Y�缫�IJ�����
��ͭ
��ͭ
���缫��Ӧʽ��Cu-2e-=Cu2+
Cu-2e-=Cu2+
����˵�������ʷ����ĵ缫��Ӧ����д������������1����ⱥ��ʳ��ˮʱ���ɵ�Դ��֪��XΪ������YΪ��������������������ʧ���ӣ��������������ӵõ��ӣ�
��2�����ݵ�⾫��ͭ�Ĺ���ԭ��֪ʶ���ش�
��2�����ݵ�⾫��ͭ�Ĺ���ԭ��֪ʶ���ش�
����⣺��1���ٺ͵�Դ�ĸ��������ĵ缫X�����������õ缫�������ӷ����õ��ӵĻ�ԭ��Ӧ����2H++2e-=H2����
�ʴ�Ϊ��2H++2e-=H2����
�ں͵�Դ�����������ĵ缫Y�����������õ缫�������ӷ���ʧ���ӵ�������Ӧ����2Cl--2e-=Cl2����
�ʴ�Ϊ��2Cl--2e-=Cl2����
����2NaOH��H2���������õ�112mL��״���µ����壬��n��OH-��=
��2=0.01mol��
c��OH-��=
=0.1mol/L������pH=13��
�ʴ�Ϊ��13��
��2���ٵ�ⷽ��������ͭ�����ص����������Ǵ�ͭ���缫��ӦΪ��Cu2++2e-=Cu���ʴ�Ϊ����ͭ��Cu2++2e-=Cu��
�ڵ�ⷽ��������ͭ�����ص����������Ǵ�ͭ���缫��ӦΪ��Cu-2e-=Cu2+���ʴ�Ϊ����ͭ��Cu-2e-=Cu2+��
�ʴ�Ϊ��2H++2e-=H2����
�ں͵�Դ�����������ĵ缫Y�����������õ缫�������ӷ���ʧ���ӵ�������Ӧ����2Cl--2e-=Cl2����
�ʴ�Ϊ��2Cl--2e-=Cl2����
����2NaOH��H2���������õ�112mL��״���µ����壬��n��OH-��=
| 0.112L |
| 22.4L/mol |
c��OH-��=
| 0.01mol |
| 0.1L |
�ʴ�Ϊ��13��
��2���ٵ�ⷽ��������ͭ�����ص����������Ǵ�ͭ���缫��ӦΪ��Cu2++2e-=Cu���ʴ�Ϊ����ͭ��Cu2++2e-=Cu��
�ڵ�ⷽ��������ͭ�����ص����������Ǵ�ͭ���缫��ӦΪ��Cu-2e-=Cu2+���ʴ�Ϊ����ͭ��Cu-2e-=Cu2+��
���������⿼��ѧ�����صĹ���ԭ��֪ʶ����ȷͼ�е�Դ��������ȷ�����ص��������ǽ��Ĺؼ�������Ϥ�缫��Ӧ�����ӵķŵ�˳���������Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
 ��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���
��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���
 ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һc��A��B������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һc��A��B������缫�壬ͨ��������ֱ����Դ��������ش��������⣺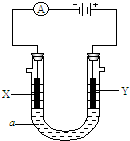 ��I��Li-SOCl2��ؿ����������������õ�صĵ缫���Ϸֱ�Ϊ﮺�̼�����Һ��LiAlCl4-SOCl2����ص��ܷ�Ӧ�ɱ�ʾΪ��4Li+2SOCl2=4LiCl+S+SO2��
��I��Li-SOCl2��ؿ����������������õ�صĵ缫���Ϸֱ�Ϊ﮺�̼�����Һ��LiAlCl4-SOCl2����ص��ܷ�Ӧ�ɱ�ʾΪ��4Li+2SOCl2=4LiCl+S+SO2�� ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ������
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ������