题目内容
【题目】下列说法正确的是( )
A. 合成氨生产中,使用高效催化剂可提高原料平衡转化率
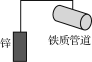
B. 铁质管道与锌用导线相连(如图所示)可防止管道被腐蚀
C. 5 mL 18 mol·L-1浓硫酸与足量铜共热,反应最多转移0.18 mol电子
D. 常温下,反应2H2S(g)+SO2(g)===3S(s)+2H2O(l)能自发进行,该反应ΔH>0
【答案】B
【解析】
A、催化剂不能使平衡移动,故使用高效的催化剂平衡不移动,原料的转化率不能改变,选项A错误;
B..导线连接锌块,构成原电池时Zn为负极,Fe作正极被保护,则可以减缓管道的腐蚀,选项B正确;
C.5mL 18molL-1浓硫酸中含有0.09mol硫酸,铜与浓硫酸的反应中,消耗0.09mol硫酸会生成0.045mol二氧化硫,转移0.09 mol电子,由于稀硫酸不与铜反应,所以反应生成的二氧化硫小于0.045mol,转移的电子小于0.09mol,选项C错误;
D、该反应△S<0,若反应能够自发进行,△H必须小于0,选项D错误;
答案选B。

【题目】草酸合铜酸钾是一种重要的化工原料,其晶体组成可表示为KxCuy(C2O4)z·wH2O。
(1)实验室用CuSO4溶液和NaOH溶液混合制备Cu(OH)2,再将所得Cu(OH)2与KHC2O4溶液混合,可制备草酸合铜酸钾晶体。
①已知室温下,Ksp[Cu(OH)2]=2.2×10-20。制备Cu(OH)2的过程中,pH=7时,溶液中c(Cu2+)=________。
②已知H2C2O4是二元弱酸。室温下,Ka1(H2C2O4)=5.4×10-2,Ka2(H2C2O4)=5.4×10-5,KHC2O4水解平衡常数的数值为____。
(2)一种测定草酸合铜酸钾晶体组成的方法如下:
步骤Ⅰ 准确称取1.770 0 g样品,充分加热,剩余固体为K2CO3与CuO的混合物,质量为1.090 0 g。
步骤Ⅱ 准确称取1.770 0 g样品,用NH4Cl溶液溶解、加水稀释,定容至100 mL。
步骤Ⅲ 准确量取步骤Ⅱ所得溶液25.00 mL于锥形瓶中,滴入指示剂,用浓度为0.050 00 mol·L-1的EDTA标准溶液滴定至终点。(已知Cu2+与EDTA反应的化学计量数之比为1∶1)。
重复上述滴定操作两次,有关数据记录如下表:
第一次滴定 | 第二次滴定 | 第三次滴定 | |
消耗EDTA标准溶液 的体积/mL | 25.92 | 24.99 | 25.01 |
①第一次滴定消耗的EDTA标准溶液的体积明显偏大,可能的原因有____(填字母)。
A. 锥形瓶水洗后未干燥
B. 滴定时锥形瓶中有液体溅出
C. 装EDTA标准溶液的滴定管水洗后未润洗
D. 开始滴定时,滴定管尖嘴部分未充满液体
②通过计算确定该样品的化学式(写出计算过程)。______________