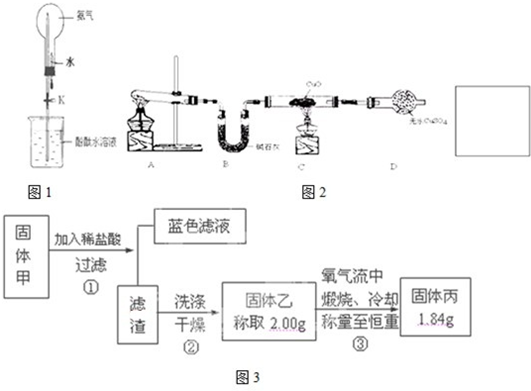
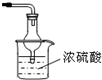
��Ŀ����
��һ����Һ�к��е����ʿ�����NaOH��NaHCO3��Na2CO3�е�һ�ֻ����֣���ȡ�����������������Һ�ֱ��Է�̪�ͼ���Ϊָʾ������ͬ��Ũ�ȵ�������еζ������ﵽ�ζ��յ�ʱ���������������ֱ�ΪV1mL ��V2mL����O<V1<V2<2V1����������Һ�е�����Ϊ
[ ]
A. NaHCO3
B.Na2CO3
C.NaHCO3��Na2CO3
D.Na2CO3��NaOH
D

��ϰ��ϵ�д�
�����Ŀ
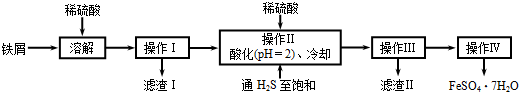
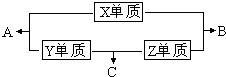 X��Y��Z��M���ֶ�����Ԫ�أ�����X��Y��Z��ԭ������֮��Ϊ16��X��Y��Z����Ԫ�صij��������ڳ��³�ѹ�¶�����ɫ���壬���ʵ��������¿��Է�������ͼ��ʾ�ı仯��
X��Y��Z��M���ֶ�����Ԫ�أ�����X��Y��Z��ԭ������֮��Ϊ16��X��Y��Z����Ԫ�صij��������ڳ��³�ѹ�¶�����ɫ���壬���ʵ��������¿��Է�������ͼ��ʾ�ı仯��