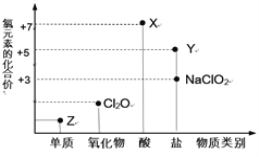
题目内容
【题目】“低碳经济”已成为全世界科学家研究的重要课题。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)已知:①CO(g)+H2O(g)![]() H2(g)+CO2(g) ΔH=-41 kJ·mol-1
H2(g)+CO2(g) ΔH=-41 kJ·mol-1
②C(s)+2H2(g)![]() CH4(g) ΔH=-73kJ·mol-1
CH4(g) ΔH=-73kJ·mol-1
③2CO(g)![]() C(s)+CO2(g) ΔH=-171 kJ·mol-1
C(s)+CO2(g) ΔH=-171 kJ·mol-1
写出CO2与H2反应生成CH4 和H2O(g)的热化学方程式: __________________。
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,在容积为2L的密闭容器中,充入1 molCO2和3.25 mol H2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:
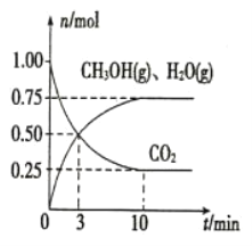
①从反应开始到平衡,氢气的平均反应速率v(H2)=_____________。
②下列措施一定不能使CO2的转化率增大的是_____________(选填编号)。
A.在原容器中再充入1molCO2
B.在原容器中再充入1molH2
C.在原容器中再充入1mol氦气
D.使用更有效的催化剂
E.缩小容器的容积
F.将水蒸气从体系中分离
(3)煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:CO(g)+H2O(g)![]() H2(g)+CO2(g)中CO的平衡转化率随
H2(g)+CO2(g)中CO的平衡转化率随![]() 及温度变化关系如图所示:
及温度变化关系如图所示:
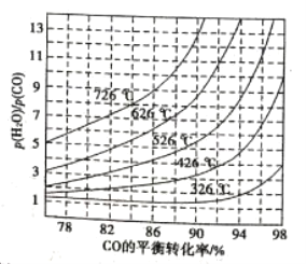
①上述反应的逆反应方向是_____________反应(填“吸热”或“放热”);
②对于气相反应,用某组分(B)的平衡分压(pB)代替平衡浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp的表达式为______________,提高![]() ,则Kp_____________(填“变大”、“变小”或“不变”)。使用铁镁催化剂的实际工业流程中,一般采用400 ℃左右、
,则Kp_____________(填“变大”、“变小”或“不变”)。使用铁镁催化剂的实际工业流程中,一般采用400 ℃左右、![]() =3~5,采用此条件的原因可能是___________。
=3~5,采用此条件的原因可能是___________。
【答案】CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H=-162 kJ·mol-1 0.1125mol·L-1·min-1 ACD 吸热
CH4(g)+2H2O(g) △H=-162 kJ·mol-1 0.1125mol·L-1·min-1 ACD 吸热 ![]() 不变 催化剂的活性温度在400℃左右;且投料比
不变 催化剂的活性温度在400℃左右;且投料比![]() =3 ~5时,CO的平衡转化率较高,成本小
=3 ~5时,CO的平衡转化率较高,成本小
【解析】
(1)根据盖斯定律②+③-2×①可知CO2与H2反应生成CH4 和H2O(g)的热化学方程式CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)△H=-162 kJ·mol-1。故答案为:CO2(g)+4H2(g)
CH4(g)+2H2O(g)△H=-162 kJ·mol-1。故答案为:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H=-162 kJ·mol-1
CH4(g)+2H2O(g) △H=-162 kJ·mol-1
(2)①用CO2来生产燃料甲醇的化学方程式为CO2+3H2![]() CH3OH+H2O,从反应开始到平衡,H2的物质的量变化了2.25mol,则物质的量浓度变化2.25mol÷2L=1.125mol/L,反应在10min时达到平衡,v(H2)=1.125 mol/L÷10min=0.1125 mol·L-1·min-1。
CH3OH+H2O,从反应开始到平衡,H2的物质的量变化了2.25mol,则物质的量浓度变化2.25mol÷2L=1.125mol/L,反应在10min时达到平衡,v(H2)=1.125 mol/L÷10min=0.1125 mol·L-1·min-1。
②A.在原容器中再充入1molCO2将使CO2的转化率降低;在原容器中再充入1molH2,反应向正反应方向移动,会使CO2的转化率升高;在原容器中再充入1mol氦气,由于体积不变,所以浓度不变,因此对反应无影响;催化剂不能改变平衡状态,只能改变反应速率;缩小容器的容积可以增大压强,由于反应中反应物的化学计量数之和大于生成物,故反应会向正反应方向移动,使CO2的转化率升高;将水蒸气从体系中分离会使反应向正反应方向移动,使CO2的转化率升高;故选ACD。
(3)①从图中可以看到,随着反应温度升高,CO的平衡转化率降低,故正反应是放热反应,所以逆反应是吸热反应。
②用平衡分压(pB)代替平衡浓度(cB)表示平衡常数Kp=![]() 。提高
。提高![]() ,对Kp无影响,故Kp不变。使用铁镁催化剂的实际工业流程中,一般采用400 ℃左右、
,对Kp无影响,故Kp不变。使用铁镁催化剂的实际工业流程中,一般采用400 ℃左右、![]() =3~5,采用此条件的原因可能是:催化剂的活性温度在400℃左右;且投料比
=3~5,采用此条件的原因可能是:催化剂的活性温度在400℃左右;且投料比![]() =3 ~5时,CO的平衡转化率较高,成本小。
=3 ~5时,CO的平衡转化率较高,成本小。

 阅读快车系列答案
阅读快车系列答案