题目内容
【题目】在某容积一定的密闭容器中,有下列可逆反应xA(g)+B(g)2C(g),反应曲线(T表示温度,P表示压强,C%表示C的体积分数)如图所示,试判断对图的说法中一定正确的是( )
A.该反应是吸热反应
B.x=2
C.P3<P4 , y轴可表示混合气体的相对分子质量
D.P3>P4 , y轴可表示C物质在平衡体积中的百分含量
【答案】D
【解析】A.根据图1可知在压强相同时T1曲线首先得到平衡状态,则T1大于T2。温度越高C的体积分数越低,这说明升高温度平衡向逆反应方向进行,则该反应是放热反应,A不符合题意;
B.根据图1可知在温度相同时P2曲线首先得到平衡状态,则P2大于P1。压强越大,C的体积分数越大,这说明增大压强平衡向正反应方向进行,即正反应是体积减小的可逆反应,但x不一定等于2,B不符合题意;
C.根据图2 可知升高温度Y减小,营业升高温度平衡向逆反应方向进行,气体的物质的量增加,而气体质量不变,则平均相对分子质量减小。由于增大压强平衡向正反应方向进行,气体的物质的量减小,质量不变,气体的平均相对分子质量增加,所以应该是P4<P3,C不符合题意;
D.由于增大压强平衡向正反应方向进行,C的百分含量增加。所以如果P3>P4,则y轴可表示C物质在平衡体积中的百分含量,D符合题意。
所以答案是:D
【考点精析】本题主要考查了化学平衡状态本质及特征的相关知识点,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)才能正确解答此题.

【题目】现有A、B、C、D、E五种元素,他们性质如下:
A | 周期表中原子半径最小的元素 |
B | 电负性最大的元素 |
C | C的2p轨道中有三个未成对的单电子 |
D | 原子核外电子数是B与C核外电子数之和 |
E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
请回答如下问题:
(1)基态E原子有_____个未成对电子,二价E离子的核外电子排布式为_______。
(2)A2D分子中D原子的杂化类型是______,D的氧化物DO3分子空间构型为_______。
(3)CA3极易溶于水,其原因主要是_____,试判断CA3溶于水后,形成CA3· H2O的合理结构:____ (填字母代号), 推理依据是_____。
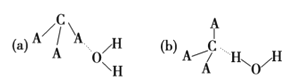
(4)在ESO4溶液中滴入过量氨水,形成配合物的颜色为______,反应的离子方程式为_____。
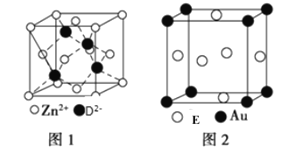
(5)ZnD的晶胞结构如图1所示,在ZnD晶胞中,D2-的配位数为______。
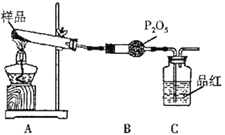
(6)E与金形成的金属互化物结构如图2所示,其晶胞边长为a nm,该金属互化物的密度为______(用含a、NA的代数式表示)g· cm-3。