题目内容
下列关于电解质溶液的正确判断是
| A.在pH=12的溶液中,K+、Cl-、HCO3-、Na+可以常量共存 |
| B.在pH=0的溶液中,Na+、NO3-、SO32-、K+可以常量共存 |
| C.由0.1 mol·L-1一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH=B++OH- |
D.由0.1 mol·L-1一元酸HA溶液的pH=3,可推知NaA溶液存在A-+H2O HA+OH- HA+OH- |
D
解析试题分析:A、pH=12的溶液显碱性,则HCO3-不能大量共存,A不正确;B、pH=0的溶液显酸性,则NO3-与SO32-之间发生氧化还原反应而不能大量共存,B不正确;C、0.1 mol·L-1一元碱BOH溶液的pH=10,可推知BOH是弱碱,溶液存在电离平衡BOH B++OH-,C不正确;D、0.1 mol·L-1一元酸HA溶液的pH=3,可推知HA是弱酸,存在电离平衡。大于相应的钠盐NaA水解,溶液存在水解平衡A-+H2O
B++OH-,C不正确;D、0.1 mol·L-1一元酸HA溶液的pH=3,可推知HA是弱酸,存在电离平衡。大于相应的钠盐NaA水解,溶液存在水解平衡A-+H2O HA+OH-,D正确,答案选D。
HA+OH-,D正确,答案选D。
考点:考查离子共存、电离平衡与水解平衡的判断与应用

练习册系列答案
相关题目
某Na2CO3、NaAlO2的混合溶液中逐滴加入1 mol/L的盐酸,测得溶液中CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是( )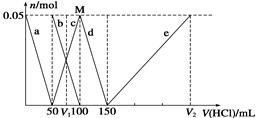
| A.原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2 |
| B.V1∶V2=l∶5 |
| C.M点时生成的CO2为0.05 mol |
| D.a曲线表示的离子方程式为AlO2-+H++H2O=Al(OH)3↓ |
已知某溶液中存在较多的 ,该溶液中还可能大量存在的离子组是
,该溶液中还可能大量存在的离子组是
A.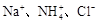 | B.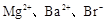 |
| C.Mg2+、Cl-、Fe2+ | D.K+、SiO 、Cl- 、Cl- |
下列各组离子一定能大量共存的是
| A.在强碱性溶液中: NH4+、Na+、NO3-、CO32- |
| B.能使紫色石蕊试液变蓝的溶液中:Ca2+、Fe2+、AlO2-、Cl- |
| C.某无色溶液中:Cu2+、Al3+、NO3-、SO42- |
| D.含有大量H+的溶液中:Na+、K+、Al3+、NO3- |
下列分子或离子在指定的分散系中能大量共存的一组是
| A.溴水溶液:Na+、K+、NO3—、CH3CHO |
| B.氢氧化钠溶液:AlO2—、K+、Cl—、NO3— |
| C.氢氧化铁胶体:H+、K+、S2—、Cl— |
| D.高锰酸钾溶液:H+、Na+、SO42—、CH3CH2OH |
下列离子方程式中正确的是
| A.Fe(OH)3滴加稀盐酸:OH- + H+=H2O |
| B.向石灰乳[Ca(OH)2]溶液通入过量的二氧化碳:Ca2++2OH- +CO2=CaCO3↓+H2O |
| C.MgCl2溶液中滴加氨水:Mg2+ + 2OH-=Mg(OH)2↓ |
| D.NaHSO4溶液中加BaCl2溶液:SO42- + Ba2+= BaSO4↓ |
下列离子方程式书写正确的是
| A.碳酸钙与醋酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
B.氯气通入水中:Cl2+H2O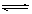 2H++Cl-+ClO- 2H++Cl-+ClO- |
| C.AlCl3溶液中加入足量的氨水:Al3++ 3NH3·H2O = Al(OH)3↓+3NH4+ |
| D.硫酸铜与氢氧化钡反应:Ba2++SO42—=BaSO4↓ |
下列解释实验事实的离子方程式不正确的是( )
| A.用烧碱溶液吸收NO2:2NO2+2OH-=NO3-+ NO2-+ H2O |
| B.用烧碱溶液吸收氯气:Cl2+2OH-=Cl-+ClO-+H2O |
| C.明矾溶液与过量氨水反应:Al3+ +3NH3.H2O=Al(OH)3↓ + 3NH4+ |
| D.酸性KI淀粉溶液久置后变蓝:4I-+O2+2H2O=2I2+4OH- |
下列离子方程式书写正确的是( )
| A.向KHSO4溶液中滴入Ba(OH)2溶液使pH=7:SO42- + H+ + Ba2+ + OH-=BaSO4↓+ H2O |
| B.少量小苏打溶液滴入Ba(OH)2溶液中:HCO3-+Ba2++OH-= BaCO3↓+H2O |
C.硫氢化钠发生水解:HS-+H2O H3O++S2- H3O++S2- |
| D.FeS固体加入到用硫酸酸化的H2O2溶液中: 2Fe2++2H++H2O2=2Fe3++2H2O |