��Ŀ����
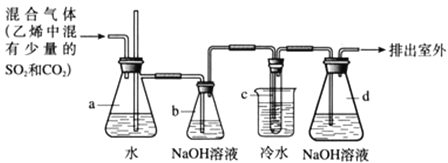
����Ŀ��1��2-���������ڳ���������ɫҺ�壬�ܶ���2.18g/cm3���е���131.4�����۵���9.79����������ˮ�������ڴ�����ͪ���л��ܼ�����ʵ���ҿ�����ͼ��ʾװ�����Ʊ�1��2-�������飮�����Թ�c��װ��Ũ��ˮ��
(1)д���Ʊ�1��2-��������Ļ�ѧ����ʽ__________________________________���÷�Ӧ����______
��Ӧ(�Ӧ����)��
(2)��ȫƿa���Է�ֹ�����������Լ��ʵ�����ʱ�Թ�c�Ƿ����������������������a�е������ǣ�____________________��
(3)����b��NaOH��Һ��������____________________��
(4)���Թ�c������ˮ�е�Ŀ����____________________��
(5)����d��NaOH��Һ��������____________________����������Ӧ�����ӷ���ʽΪ
________________________________________________________________________��
���𰸡� CH2=CH2+Br2��CH2BrCH2Br �ӳ� a�в�������ˮ������������ˮ����� ��ȥ��ϩ�е�CO2��SO2 ������Ļӷ� ���������� Br2+2OH-=Br-+BrO-+H2O
��������������Ҫ����ʵ�����Ʊ�1��2-���������ʵ�鷽����
(1)�Ʊ�1��2-��������Ļ�ѧ����ʽ��CH2=CH2+Br2��CH2BrCH2Br���÷�Ӧ���ڼӳɷ�Ӧ��
(2)�������������a����ѹ���������ǣ�a�в�������ˮ������������ˮ�������
(3)����b��NaOH��Һ�������dz�ȥ��ϩ�е�CO2��SO2��
(4)���ӷ������Թ�c������ˮ�е�Ŀ���Ǽ�����Ļӷ���
(5)����d��NaOH��Һ����������������������������Ӧ���������������Ƶķ�Ӧ���ƣ���Ӧ�����ӷ���ʽΪBr2+2OH-=Br-+BrO-+H2O��

 ������������ϵ�д�
������������ϵ�д�