题目内容
(8分)(2009·山东卷)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)合成氨反应N2(g)+3H2(g) ===2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡________移动(填“向左”“向右”或“不”);使用催化剂________反应的ΔH(填“增大”“减小”或“不改变”)。
(2)已知:O2(g)===O2+(g)+e-
ΔH1=1175.7 kJ·mol-1①
PtF6(g)+e-===PtF6-(g)
ΔH2=-771.1 kJ·mol-1②
O2+PtF6-(s)===O2+(g)+PtF6-(g)
ΔH3=482.2 kJ·mol-1③
则反应O2(g)+PtF6(g)===O2+PtF6-(s)的ΔH=________kJ·mol-1。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式),生成该沉淀的离子方程式为________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=________。
(1)合成氨反应N2(g)+3H2(g) ===2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡________移动(填“向左”“向右”或“不”);使用催化剂________反应的ΔH(填“增大”“减小”或“不改变”)。
(2)已知:O2(g)===O2+(g)+e-
ΔH1=1175.7 kJ·mol-1①
PtF6(g)+e-===PtF6-(g)
ΔH2=-771.1 kJ·mol-1②
O2+PtF6-(s)===O2+(g)+PtF6-(g)
ΔH3=482.2 kJ·mol-1③
则反应O2(g)+PtF6(g)===O2+PtF6-(s)的ΔH=________kJ·mol-1。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式),生成该沉淀的离子方程式为________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=________。
(1)向左 不改变
(2)-77.6
(3)Cu(OH)2 Cu2++2NH3·H2O===Cu(OH)2↓+2NH4+
(4)中 mol·L-1
(2)-77.6
(3)Cu(OH)2 Cu2++2NH3·H2O===Cu(OH)2↓+2NH4+
(4)中 mol·L-1
本题考查化学平衡的移动、热化学方程式、溶解平衡、溶液中离子浓度大小比较等知识,意在考查考生运用化学基本理论知识的能力。(1)在恒温、恒压条件下向平衡体系中通入氩气,容器体积增大,反应气体的浓度减小,平衡将向气体物质的量增大的方向移动,即向左移动。
(2)根据盖斯定律,ΔH=ΔH1+ΔH2-ΔH3=-77.6 kJ·mol-1。
(3)Ksp[Mg(OH)2]>Ksp[Cu(OH)2],MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成Cu(OH)2沉淀。
(4)因为氨水与盐酸反应后,生成氯化铵溶液,依据电荷守恒得c(NH4+)+c(H+)=c(Cl-)+c(OH-),由于c(NH4+)=c(Cl-),故c(H+)=c(OH-),所以溶液呈中性;NH3·H2O的电离常数Kb== mol/L。
(2)根据盖斯定律,ΔH=ΔH1+ΔH2-ΔH3=-77.6 kJ·mol-1。
(3)Ksp[Mg(OH)2]>Ksp[Cu(OH)2],MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成Cu(OH)2沉淀。
(4)因为氨水与盐酸反应后,生成氯化铵溶液,依据电荷守恒得c(NH4+)+c(H+)=c(Cl-)+c(OH-),由于c(NH4+)=c(Cl-),故c(H+)=c(OH-),所以溶液呈中性;NH3·H2O的电离常数Kb== mol/L。

练习册系列答案
相关题目
 SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。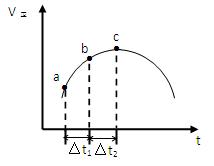
 bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。
bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。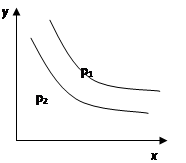
 C(g)+D(g),当下列物理量不发生变化时: ①混合气体的密度 ②容器内气体的压强 ③混合气体的平均相对分子质量 ④B的物质的量浓度 能表明该反应一定已达到平衡状态的是 ( )
C(g)+D(g),当下列物理量不发生变化时: ①混合气体的密度 ②容器内气体的压强 ③混合气体的平均相对分子质量 ④B的物质的量浓度 能表明该反应一定已达到平衡状态的是 ( ) NaCl(l)+ K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+ K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来
 ,若要提高CO的转化率,下列措施中可行的是 ( )
,若要提高CO的转化率,下列措施中可行的是 ( )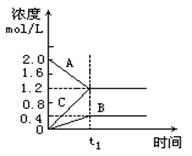
 Fe(SCN)3+3NH4Cl溶液显红色,加少量NH4Cl固体后颜色变浅
Fe(SCN)3+3NH4Cl溶液显红色,加少量NH4Cl固体后颜色变浅